Тромбоцитопения: Симптомы, диагностика и лечение
Тромбоцитопения — это термин, обозначающий все состояния, при которых снижено количество тромбоцитов в крови. Человек может чувствовать себя вполне нормально, однако, такое состояние при тромбоцитопении опасно, так как в любой момент может произойти внутреннее кровотечение любых органов, а самое опасное то, что может случиться кровоизлияние в мозг.
Патология встречается чаще у женщин,чем у мужчин. Частота выявления у детей — один случай на 20 тысяч.
Причины
Зачастую причиной заболевания является аллергическая реакция организма на различные медицинские препараты в итоге чего и наблюдается лекарственная тромбоцитопения. При таком недомогании наблюдается выработка организмом антител, направленных против лекарственного препарата. К лекарственным препаратам, влияющим на появление кровеносной недостаточности телец, относятся седативные, алкалоидные и антибактериальные средства.
Причинами возникновения недостаточности могут быть и проблемы с иммунитетом, вызванные последствиями переливаний крови. Особенно часто заболевание проявляется при несовпадении групп крови.
Чаще всего наблюдается в организме человека аутоиммунная тромбоцитопения. В таком случае иммунитет неспособен к распознаванию своих тромбоцитов и отторгает их из организма. В результате отторжения происходит выработка антител по удалению чужеродных клеток.
Если же недуг имеет выраженную форму изолированной болезни, то он именуется идиопатической тромбоцитопенией или заболеванием Верльгофа. Считается, что такая тромбоцитопения возникает на фоне наследственной предрасположенности.
Также свойственно проявление заболевания при наличии врождённого иммунодефицита.
Недостаток тромбоцитов в организме наблюдается у людей, с пониженным составом витамина В12 и фолиевой кислоты. Не исключается и чрезмерное радиоактивное или лучевое воздействие для появления недостаточности кровяных телец.
Симптомы
Обычно первым сигналом снижения уровня тромбоцитов служит появление кожных кровоизлияний при незначительном травмировании (ударе, сдавлении) мягких тканей. Больные отмечают частое возникновение синяков, специфической мелкоточечной сыпи на теле и конечностях, кровоизлияний в слизистые оболочки, повышенную кровоточивость десен и т. п.
На следующем этапе отмечается увеличение времени кровотечения при незначительных порезах, длительные и обильные менструальные кровотечения у женщин, появление экхимозов в местах инъекций. Кровотечение, вызванное травмой или медицинской манипуляцией (например, удалением зуба) может продолжаться от нескольких часов до нескольких суток.
При значительном снижении количества тромбоцитов возникают спонтанные кровотечения (носовые, маточные, легочные, почечные, желудочно-кишечные), выраженный геморрагический синдром после хирургических вмешательств. Профузные некупируемые кровотечения и кровоизлияния в мозг могут стать фатальными.
Диагностика
Прежде всего, при подозрении на тромбоцитопению необходимо сделать общий анализ крови для определения количества клеточных элементов и верификации (подтверждения) диагноза тромбоцитопения.
Многие заболевания, протекающие с тромбоцитопенией, имеют достаточно яркие симптомы, поэтому дифференциальная диагностика в таких случаях не представляет большого труда. Это касается, в первую очередь, тяжелых онкологических патологий (лейкозы, метастазы злокачественных опухолей в костный мозг, миеломная болезнь и т.п.), системных заболеваний соединительной ткани (системная красная волчанка), цирроза печени и т.п.
Однако нередко необходимо проведение дополнительных исследований (пункция костного мозга, иммунологические пробы и т.п.).
Лечение
Кровотечения при легкой степени тромбоцитопении не развиваются. Медикаментозное лечение, как правило, не требуется. Рекомендуется выжидательная тактика и установление причины снижения тромбоцитов.
При средней тяжести заболевания возможно появление кровоизлияний в слизистую оболочку рта, повышение кровоточивости десен, учащение носовые кровотечений. При ушибах и травмах могут образовываться обширные кровоизлияния в кожу, не соответствующие объему повреждения. Медикаментозная терапия рекомендуется только в случае наличия факторов, повышающих риск развития кровотечений (язв желудочно-кишечной системы, профессиональной деятельности или спорта, связанного с частыми травмами).
При ушибах и травмах могут образовываться обширные кровоизлияния в кожу, не соответствующие объему повреждения. Медикаментозная терапия рекомендуется только в случае наличия факторов, повышающих риск развития кровотечений (язв желудочно-кишечной системы, профессиональной деятельности или спорта, связанного с частыми травмами).
При тромбоцитопении средней степени тяжести без выраженных проявлений геморрагического синдрома назначается лечение на дому. Пациентам рекомендуется ограничить активный образ жизни на период лечения и принимать все медикаменты, назначенные гематологом.
Обязательной госпитализации подлежат пациенты с тяжелой степенью тромбоцитопении. Таким больным, помимо медикаментозного, могут быть назначены различные терапевтические и хирургические мероприятия, направленные на устранение тромбоцитопении и вызвавших ее причин.
Дополнительными методами лечения тромбоцитопении являются: трансфузионная терапия (переливание пациенту донорской крови, плазмы либо тромбоцитов), удаление селезенки и пересадка костного мозга.
Тромбоцитопения у детей
Кровь человека состоит из таких элементов – лимфоциты, тромбоциты и эритроциты. Тромбоциты принимают участие в свертываемости крови. Норма для одного микролитра – 150–400 пластинок. Если число тромбоцитов становится менее 100 единиц, то это говорит о развитии такого заболевания крови, как тромбоцитопения. Для ребенка с этой болезнью любая травма становится опасной для жизни, так как при этом может быть значительная потеря крови. Диагноз – тромбоцитопения у ребенка ставится довольно редко, в основном у младших школьников (5 человек на 100 000). О причинах появления и способах лечения детей мы сейчас расскажем.
Причины и типы заболевания
Детская форма тромбоцитопении (пурпуры) подразделяется на 2 вида – врожденная и приобретенная. У новорожденных диагностируются такие синдромы, как:
- Бернара-Сулье;
- гиперспленизм;
- Мея-Хегглина;
- Фраскони;
- Вискота-Олдрича.
Причиной образования врожденных патологий являются наследственные факторы, попадание в организм беременной аутоантител, инфекций и вирусов.
Причины приобретенных типов заболевания различные. Это, в частности, отравления, аллергии на лекарства, а также патологическое усиление функции селезенки. Часто у детей заболевание развивается после прививки под названием инфанрикс. Она призвана защищать от таких болезней, как:
- коклюш;
- гепатит;
- менингит;
- полиомиелит;
- дифтерия;
- столбняк.
Тромбоцитопения у детей иногда развивается при онкологиях. Также болезнь может появиться у малыша после перенесенного мононуклеоза. Эта опасная патология вызывает осложнения в виде нарушения работы селезенки, а иногда даже ее разрыв.
Симптомы тромбоцитопении у детей
Заболевание коварно тем, что проходит безболезненно и состояние ребенка при этом не изменяется. Родители могут длительное время не замечать признаков, а при прогрессировании может появиться внутреннее кровотечение, которое опасно для жизни. Нужно срочно посетить врача и пройти процедуру обследования, если появились такие симптомы:
- мелкие точки на ногах, реже в других местах на коже (такое проявление есть у 100% больных), от этого и произошло название – пурпура;
- регулярные носовые кровоизлияния;
- часто идет кровь из десен;
- изредка кровяные следы в кале или его черный цвет;
- появление синяков после незначительных ударов;
- кровь долго не перестает течь из небольших царапин на коже.

Самыми опасными являются кровотечения в мозге и во внутренних органах.
Установление диагноза
Большое значение имеет исследование крови ребенка. Выполняется не только аппаратный анализ, но также визуальный осмотр и подсчет клеток под микроскопом. При лабораторном анализе обнаруживается уменьшение количества тромбоцитов в плацентарной массе. Иногда при проведении УЗИ выявляется, что увеличена селезенка.
В некоторых случаях осуществляется пункция мозга. Ее делают при длительном заболевании или его рецидиве. Также врачом по необходимости назначается обследование сердца с помощью электрокардиограммы, рентгеновские исследования, анализ крови на антитела, генетический тест и эндоскопия.
Методы лечения тромбоцитопении у детей
При легкой форме болезни доктор назначит диетическое питание и тщательное наблюдение за маленьким пациентом. В рационе должны присутствовать:
- растительные белки;
- бульон из курицы;
- рыба;
- свежие овощи в салатах с растительными маслами;
- продукты, содержащие фолиевую кислоту, цианокобаломин, витамины С и В12;
- каши и макароны.

Лечение тромбоцитопении медикаментами не требуется. Желательно давать ребенку травяные чаи из таких растений, как крапива, тысячелистник, водяной перец, а также из плодов калины.
В более тяжелых случаях назначаются глюкокортикостероиды, препараты, увеличивающие число тромбоцитов в крови и предотвращающие их распад в селезенке. Иногда результативным является переливание крови от ближайших родственников. Это лечение назначается однократно, при повторной процедуре увеличивается выработка антител. Существуют и другие методы, их назначит врач.
Тромбоцитопения у детей, лечение которой зависит от причины появления болезни, требует большого внимания и участия взрослых, а иногда и временной изоляции ребенка. Нужно уметь быстро оказать ему первую помощь при кровотечении, а более взрослого ребенка ознакомить с правилами безопасного поведения. Он также должен уметь быстро остановить самостоятельно кровь. Важно, избегать аллергенов, беречь малыша от инфекционных и простудных заболеваний. Заботьтесь о своих близких и будьте здоровы!
Заботьтесь о своих близких и будьте здоровы!
Иммунные тромбоцитопении у новорожденных детей: трудности диагностики и тактика ведения | Заплатников, Карасева Л.Н., Подкопаев В.Н., Фомина С.Г., Шипулина О.Ю., Домонова Э.А., Садова Н.В.
Иммунные тромбоцитопении у новорожденных детей:трудности диагностики и тактика ведения
Геморрагические нарушения у новорожденных детей из-за высокого риска тяжелых осложнений и неблагоприятных исходов относят к ургентным состояниям. При этом в неонатологической практике геморрагический синдром по-прежнему остается одним из наиболее сложных для нозологической верификации [1–3].Долгие годы большинство геморрагических расстройств в неонатальный период связывали с дефицитом витамин К-зависимых факторов свертывания (геморрагическая болезнь новорожденного), ДВС-синдромом, тяжелыми врожденными и постнатальными инфекциями, наследственными коагулопатиями. В дальнейшем результаты исследований (1970–1990 гг.) показали, что причинами неонатального геморрагического синдрома могут быть и другие патологические состояния, в т. ч. и иммуно-опосредованные тромбоцитопении [4].
ч. и иммуно-опосредованные тромбоцитопении [4].
Ранее нами совместно с сотрудниками лаборатории иммуногематологии Гематологического научного центра РАМН был представлен алгоритм диагностики иммунных тромбоцитопений у новорожденных детей [5, 6]. Однако анализ клинических наблюдений и результаты тестирования врачей, проводимого нами в рамках циклов повышения квалификации, свидетельствуют о том, что практикующие неонатологи и педиатры все еще недостаточно информированы о роли иммунно-опосредованных тромбоцитопений в развитии геморрагического синдрома у новорожденных. Недооценка этиологического значения иммунной тромбоцитопении в генезе неонатальных геморрагических нарушений может стать причиной диагностической ошибки и неадекватного лечения. В качестве примера приводим собственное клиническое наблюдение.
Ребенок М. (девочка). Поступила в Тушинскую детскую больницу (в настоящее время – ДГКБ им. З.А. Башляевой ДЗ г. Москвы) в возрасте 3-х сут с направляющим диагнозом «внутриутробная цитомегаловирусная инфекция (ЦМВИ) с тромбоцитопенией и геморрагическим синдромом». Ребенок от молодых, здоровых родителей. Беременность первая, желанная, протекала без особенностей. Роды на 39–40 нед., физиологические, в головном предлежании. Масса при рождении – 3450 г, длина тела – 53 см. Оценка по Апгар – 8/9 баллов. К груди приложена сразу после рождения. Грудь взяла активно. В 1-е сут жизни на фоне удовлетворительного состояния ребенка на коже появились спонтанные петехиальные элементы сыпи, а также «синячки» в местах сдавления кожи пеленками. Срочно были введены менадиона натрия бисульфит и этамзилат, отобраны пробы для клинического анализа крови и коагулограммы. Результаты обследования:
Ребенок от молодых, здоровых родителей. Беременность первая, желанная, протекала без особенностей. Роды на 39–40 нед., физиологические, в головном предлежании. Масса при рождении – 3450 г, длина тела – 53 см. Оценка по Апгар – 8/9 баллов. К груди приложена сразу после рождения. Грудь взяла активно. В 1-е сут жизни на фоне удовлетворительного состояния ребенка на коже появились спонтанные петехиальные элементы сыпи, а также «синячки» в местах сдавления кожи пеленками. Срочно были введены менадиона натрия бисульфит и этамзилат, отобраны пробы для клинического анализа крови и коагулограммы. Результаты обследования:
– клинический анализ крови (1-е сут жизни): гемоглобин – 194 г/л, эритроциты – 5,12х1012/л, MCH – 31 пг, MCV – 99 фл, лейкоциты – 17,5х109/л, нейтрофилы – 58%, лимфоциты – 32%, моноциты – 7%, эозинофилы – 2%, базофилы – 1%, тромбоциты – 63х109/л, MРV – 10 фл;
– клинический анализ крови (2-е сут жизни): гемоглобин – 181 г/л, эритроциты – 4,25х1012/л, MCH – 30 пг, MCV – 100 фл, лейкоциты – 15,1х109/л, нейтрофилы – 61%, лимфоциты – 28%, моноциты – 9%, эозинофилы – 2%, тромбоциты – 54х109/л, MРV – 11 фл;
– коагулограмма (1-е сут жизни): активированное частичное тромбопластиновое время (АЧТВ) – 34 с, протромбиновый индекс (ПТИ) – 105%, тромбиновое время – 16 с, фибриноген – 3,1 г/л;
– общий анализ мочи, биохимический анализ крови, УЗИ внутренних органов и головного мозга – без патологических изменений;
– результаты ИФА: anti-CMV-IgM – не обнаружены, anti-CMV-IgG – обнаружены: 10,2 (норма – до 4). К остальным возбудителям TORCH-синдрома специфические иммуноглобулины (Ig) выявлены не были.
К остальным возбудителям TORCH-синдрома специфические иммуноглобулины (Ig) выявлены не были.
Наличие у ребенка anti-CMV-IgG расценили как проявление внутриутробной ЦМВИ, протекающей с тромбоцитопенией и геморрагиями. Несмотря на терапию менадионом натрия бисульфитом и этамзилатом геморрагический синдром сохранялся. Для проведения специфической антицитомегаловирусной терапии ребенок был переведен в Тушинскую детскую больницу на 3-е сут жизни.
Состояние ребенка при поступлении – средней тяжести. Масса тела – 3390 г. Температура тела – 36,7°С. Частота сердечных сокращений – 138/мин, частота дыханий – 31/мин. Признаков дыхательной и сердечной недостаточности нет. Кормится сцеженным материнским молоком, сосет активно. Уровень бодрствования – адекватный. Крик громкий, не раздраженный. Рефлексы новорожденного вызываются. На коже лица, туловища, конечностей – петехиальная сыпь, единичные «синячки». На видимых слизистых – единичные петехии. Тургор тканей и эластичность кожи не нарушены. Периферические лимфатические узлы не увеличены. В легких пуэрильное дыхание. Тоны сердца ритмичные, звучные. Живот мягкий, доступен пальпации, безболезненный. Печень +1,5 см, селезенка не пальпируется. Пупочная ранка – с геморрагической корочкой, кожный валик не воспален. Пупочные сосуды не пальпируются. Стул и мочеиспускание в норме.
Периферические лимфатические узлы не увеличены. В легких пуэрильное дыхание. Тоны сердца ритмичные, звучные. Живот мягкий, доступен пальпации, безболезненный. Печень +1,5 см, селезенка не пальпируется. Пупочная ранка – с геморрагической корочкой, кожный валик не воспален. Пупочные сосуды не пальпируются. Стул и мочеиспускание в норме.
Таким образом, ведущим в клинической картине являлся геморрагический синдром, генез которого необходимо было уточнить. Для этого сразу при поступлении сito! были проведены клинический анализ крови, коагулограмма, исследование электролитов, газов крови и ее кислотно-щелочного состояния (КЩС), рентген органов грудной клетки, а также, учитывая риск внутричерепного кровоизлияния, – нейросонография и осмотр глазного дна. Одновременно был осуществлен забор крови для биохимического анализа, определения уровня С-реактивного белка (СРБ) и прокальцитонина, исследований методами полимеразной цепной реакции (ПЦР) и иммуноферментного анализа (ИФА) для верификации маркеров TORCH-инфекции (исследование проводили в ЦНИИ эпидемиологии Роспотребнадзора). Принимая во внимание тот факт, что результаты ПЦР и ИФА на внутриутробные инфекции будут известны только через 24 ч, одновременно были отобраны образцы крови ребенка, матери и отца для исключения иммунных вариантов тромбоцитопении (исследование проводили в лаборатории иммуногематологии Гематологического научного центра РАМН).
Принимая во внимание тот факт, что результаты ПЦР и ИФА на внутриутробные инфекции будут известны только через 24 ч, одновременно были отобраны образцы крови ребенка, матери и отца для исключения иммунных вариантов тромбоцитопении (исследование проводили в лаборатории иммуногематологии Гематологического научного центра РАМН).
Результаты обследования сito!:
– клинический анализ крови (3-и сут жизни): гемоглобин – 179 г/л, эритроциты – 4,31х1012/л, MCH – 29 пг, MCV – 98 фл, лейкоциты – 14,7х109/л, нейтрофилы – 56%, лимфоциты – 32%, моноциты – 8%, эозинофилы – 3%, базофилы – 1%, тромбоциты – 37х109/л, MРV – 11 фл;
– коагулограмма (3-и сут жизни: АЧТВ – 32 с, ПТИ – 113%, тромбиновое время – 15 с, фибриноген – 3,2 г/л, Хагеман-зависимый фибринолиз – 10 мин, D-димеры – 450;
– нейросонография, рентген органов грудной клетки, глазное дно, электролиты, газы крови и ее КЩС – без особенностей;
– СРБ, прокальцитонин – в пределах нормы.
При заборе капиллярной крови для клинического анализа, газов крови и ее КЩС отмечена пролонгация длительности кровоточивости.
Отсутствие изменений в коагулограмме в динамике (в 1-й и 3-й дни жизни) позволило сделать заключение, что причиной геморрагического синдрома у ребенка является тромбоцитопения без участия нарушений плазменного гемостаза. Тромбоцитопения в периоде новорожденности встречается при целом ряде патологических состояний, поэтому дифференциальный диагноз нередко вызывает затруднения. Определенная практическая помощь при этом может быть получена, если все неонатальные тромбоцитопении разделить на 2 основные патогенетические группы: иммунные и неиммунные (рис. 1).
Причинами неиммунных тромбоцитопений являются внутриутробные и тяжелые постнатальные инфекции, тромбогеморрагические синдромы, врожденный лейкоз, врожденная аплазия костного мозга (анемия Фанкони, синдром фокомелии, синдром Ландольда и др.) и другая синдромальная патология различного генеза (синдром Казабаха – Меррита, синдром Вискотта – Олдрича и др.).
В основе неонатальных иммунных тромбоцитопений лежит передача плоду через плаценту от матери антитромбоцитарных антител. При этом характер антител зависит от патогенеза иммунных изменений в организме матери. Если у матери имеет место аутоиммунная тромбоцитопения или системная красная волчанка, то существует риск трансплацентарного проникновения в организм плода аутоиммунных тромбоцитарных антител. При этом развивается так называемая трансиммунная форма неонатальной тромбоцитопении. В тех же случаях, когда плод наследует от отца тромбоцитарные антигены человека (HPA – Нuman Рlatelet Аntigens), отсутствующие у матери, возможны ее сенсибилизация и последующая передача антител плоду через плаценту с развитием алло-(изо)иммунной неонатальной тромбоцитопении (рис. 1). Значительно реже тромбоцитопении у новорожденных вызываются медикаментами, которые принимает мать (толбутамид, гидралазин, гидантион, азатиоприн, гепарин и др.) или новорожденный (жировые эмульсии для парентерального питания, вальпроаты, гепарин), а также другими причинами.
При этом характер антител зависит от патогенеза иммунных изменений в организме матери. Если у матери имеет место аутоиммунная тромбоцитопения или системная красная волчанка, то существует риск трансплацентарного проникновения в организм плода аутоиммунных тромбоцитарных антител. При этом развивается так называемая трансиммунная форма неонатальной тромбоцитопении. В тех же случаях, когда плод наследует от отца тромбоцитарные антигены человека (HPA – Нuman Рlatelet Аntigens), отсутствующие у матери, возможны ее сенсибилизация и последующая передача антител плоду через плаценту с развитием алло-(изо)иммунной неонатальной тромбоцитопении (рис. 1). Значительно реже тромбоцитопении у новорожденных вызываются медикаментами, которые принимает мать (толбутамид, гидралазин, гидантион, азатиоприн, гепарин и др.) или новорожденный (жировые эмульсии для парентерального питания, вальпроаты, гепарин), а также другими причинами.
С учетом сохраняющегося геморрагического синдрома у обсуждаемого ребенка, а также снижения уровня тромбоцитов в динамике было принято решение о необходимости проведения терапии Ig для в/в введения (ИГВВ), не дожидаясь получения результатов иммуногематологических исследований методами ИФА и ПЦР. ИГВВ человека нормальный был назначен из расчета 400 мг/кг на 1 введение, на курс – 5 введений с интервалом 24 ч; курсовая доза – 2 г/кг.
ИГВВ человека нормальный был назначен из расчета 400 мг/кг на 1 введение, на курс – 5 введений с интервалом 24 ч; курсовая доза – 2 г/кг.
Одновременно с ИГВВ-терапией продолжали проводить дифференциальную диагностику. Анализ данных анамнеза, клинической картины и результатов проведенного обследования уже в 1-е сут пребывания ребенка в Тушинской детской больнице позволил исключить сепсис и некротизирующий энтероколит, тромбогеморрагические синдромы, анемию Фанкони, синдром фокомелии, синдром Казабаха – Меррита, а также побочные действия медикаментов (табл. 1).
Полученные в дальнейшем результаты обследования на TORCH-инфекции свидетельствовали об отсутствии маркеров внутриутробных инфекций. Так, были получены отрицательные результаты ПЦР-анализа (кровь, моча) на вирусы герпеса человека 1, 2, 6-го типов, цитомегаловирус (ЦМВ), вирус краснухи, токсоплазму. Результаты ИФА-анализа свидетельствовали об отсутствии в сыворотке крови ребенка специфических антител к герпес-вирусам, вирусу краснухи, токсоплазме, а также anti-CMV-IgM. Выявленные anti-CMV-IgG были высокоавидными (0,78) и сопоставимыми с материнскими по титру и авидности, что, наряду с отсутствием генома ЦМВ в биологических средах ребенка, позволило исключить у него внутриутробную ЦМВИ. С учетом особенностей обнаруженных в сыворотке крови ребенка антител к ЦМВ (Ig класса G, концентрация и индекс авидности – как у матери) они были расценены как материнские, переданные ребенку трансплацентарно. Таким образом, предположение о внутриутробной ЦМВИ как причине тромбоцитопении не нашло убедительных подтверждений.
Выявленные anti-CMV-IgG были высокоавидными (0,78) и сопоставимыми с материнскими по титру и авидности, что, наряду с отсутствием генома ЦМВ в биологических средах ребенка, позволило исключить у него внутриутробную ЦМВИ. С учетом особенностей обнаруженных в сыворотке крови ребенка антител к ЦМВ (Ig класса G, концентрация и индекс авидности – как у матери) они были расценены как материнские, переданные ребенку трансплацентарно. Таким образом, предположение о внутриутробной ЦМВИ как причине тромбоцитопении не нашло убедительных подтверждений.
В то же время результаты иммуногематологического исследования наглядно продемонстрировали наличие в сыворотках крови матери и ребенка антител к тромбоцитам ребенка и его отца (рис. 2). Это позволило сделать вывод о том, что причиной геморрагического синдрома в данном случае является аллоиммунная тромбоцитопения, развившаяся в результате изоиммунизации матери HPA плода, который унаследовал их от отца. ИГВВ-терапия была продолжена, что позволило быстро купировать геморрагический синдром и добиться тенденции к восстановлению уровня тромбоцитов (112х109/л – на 7–е сут жизни, после 5-го введения ИГВВ; 141х109/л – к 10–м сут жизни; 148х109/л – к 14-м сут жизни; 164х109/л – к 21-м сут жизни). Катамнестическое наблюдение за ребенком в дальнейшем свидетельствует об отсутствии тромбоцитопении и геморрагического синдрома.
Катамнестическое наблюдение за ребенком в дальнейшем свидетельствует об отсутствии тромбоцитопении и геморрагического синдрома.
Таким образом, в структуре неонатальных тромбоцитопений особое место занимают иммунные варианты. При этом трансиммунные неонатальные тромбоцитопении наблюдаются в тех случаях, когда у матерей имеет место аутоиммунная тромбоцитопения или системная красная волчанка. В основе патогенеза данной формы неонатальной тромбоцитопении лежит трансплацентарный перенос к плоду материнских аутоиммунных антитромбоцитарных антител класса IgG. По данным разных авторов, у женщин с аутоиммунной тромбоцитопенией риск рождения ребенка с трансиммунной неонатальной тромбоцитопенией достигает 30–75%. При этом тяжелые формы тромбоцитопении отмечаются в 8–15% случаев, а риск внутричерепного кровоизлияния составляет 1,5% [8]. Доказано, что степень снижения уровня тромбоцитов у матери во время беременности не влияет на тяжесть трансиммунной неонатальной тромбоцитопении. К сожалению, до настоящего времени нет единой и общедоступной тактики ведения беременных с аутоиммунной тромбоцитопенией, позволяющей эффективно и безопасно профилактировать развитие трансиммунной неонатальной тромбоцитопении.
Верификация диагноза трансиммунной тромбоцитопении проводится на основании результатов иммуногематологического обследования, в основе которого лежит проведение проб совместимости сыворотки ребенка, матери, отца с тромбоцитами, соответственно, ребенка, матери, отца. Если отмечается взаимодействие сыворотки матери с собственными тромбоцитами, а также с тромбоцитами ребенка и отца и одновременно сыворотка ребенка взаимодействует со своими собственными тромбоцитами, а также с тромбоцитами матери и тромбоцитами отца, то подтверждается трансиммунный вариант (рис. 3). Объясняется это тем, что аутоиммунные антитромбоцитарные антитела матери передаются ребенку через плаценту и еще несколько недель и даже месяцев после рождения будут циркулировать в его кровотоке. Аутоиммунные антитела направлены против общих HPA, присутствующих на тромбоцитах всех людей, и сыворотки крови, в которых они находятся (в данном случае – в материнской и у новорожденного), будут взаимодействовать с тромбоцитами не только матери, ребенка, но и отца. В связи с тем, что в сыворотке крови отца аутоиммунных антитромбоцитарных антител нет, она не взаимодействует ни с собственными тромбоцитами, ни с тромбоцитами ребенка и матери (рис. 3).
В связи с тем, что в сыворотке крови отца аутоиммунных антитромбоцитарных антител нет, она не взаимодействует ни с собственными тромбоцитами, ни с тромбоцитами ребенка и матери (рис. 3).
Изоиммунная (аллоиммунная) тромбоцитопения встречается с частотой 1 случай на 1 тыс. новорожденных [8]. Патогенез последней во многом сходен с механизмом развития гемолитической анемии новорожденных при резус-конфликте и является результатом проникновения через плаценту к матери тромбоцитов плода. При несовместимости матери и плода по HPA женщина иммунизируется и вырабатывает антитела к антигенам плода, которых нет на ее тромбоцитах, но они унаследованы ребенком от отца. В подавляющем большинстве случаев изосенсибилизация матери происходит к антигену НPА-1а. Образовавшиеся в организме беременной антитела класса IgG к HPA плода в последующем передаются через плаценту и связываются с тромбоцитами плода, что приводит к их повышенному разрушению уже внутриутробно. При этом установлено, что в половине всех случаев внутричерепных геморрагий, обусловленных изоиммунной (аллоиммунной) тромбоцитопенией, кровоизлияния развиваются еще внутриутробно. В целом риск внутричерепных кровоизлияний при данной форме иммунной неонатальной тромбоцитопении, по некоторым данным, достигает 20% [8].
В целом риск внутричерепных кровоизлияний при данной форме иммунной неонатальной тромбоцитопении, по некоторым данным, достигает 20% [8].
Показано, что развитие изоиммунной (аллоиммунной) тромбоцитопении возможно даже при первой беременности, но наиболее тяжелое течение заболевания отмечается при последующих беременностях от этого же партнера. В связи с этим в случае выявления у новорожденного изоиммунной тромбоцитопении родители должны быть предупреждены о высоком риске рождения детей с тяжелыми формами заболевания. При этом единых подходов к ведению беременных, изоиммунизированных к НPА, нет, но большинство исследователей придерживаются тактики еженедельного введения ИГВВ в дозе 1 г/кг, в некоторых случаях в комбинации с глюкокортикоидами (0,5 мг/кг по преднизолону), начиная с 20-й нед. гестации. Следует отметить, что в ряде клиник достигнуты хорошие результаты при мониторировании уровня тромбоцитов у плодов в пуповинной крови для выявления тех критических случаев тромбоцитопении, когда необходимо внутрипуповинное (под УЗИ-контролем) введение ИГВВ и тромбоцитарного концентрата.
Диагностика изоиммунной (аллоиммунной) тромбоцитопении основана на уточнении анамнеза (указание на предшествующую беременности изоиммунизацию матери из-за неоднократного переливания тромбоцитов и/или рождение детей с изоиммунной тромбоцитопенией), а также результатов иммуно-гематологического обследования. При этом взаимодействие сыворотки крови матери и ребенка с тромбоцитами ребенка и отца при отсутствии взаимодействия их с тромбоцитами матери свидетельствует об изоиммуной (аллоиммунной) тромбоцитопении. Объяснением этому является тот факт, что антитромбоцитарные антитела матери, выработанные на отсутствующий у нее антиген, но имеющийся у ребенка (унаследован от отца), трансплацентарно передаются плоду. Таким образом, сыворотка крови матери и сыворотка крови ребенка содержат эти антитела, мишенью для которых являются тромбоциты ребенка и отца (рис. 2).
Тактика ведения новорожденных детей с иммунными тромбоцитопениями предусматривает необходимость обязательного ежедневного контроля за количеством тромбоцитов в течение раннего неонатального периода. При тяжелой тромбоцитопении обязательны также контроль за неврологическим статусом новорожденного, проведение нейросонографии и осмотр глазного дна в динамике. В тех случаях, когда количество тромбоцитов снижается до 50х109/л и ниже, а геморрагический синдром прогрессирует, показано назначение ИГВВ. Доказано, что терапевтический эффект ИГВВ достигается при курсовой дозе 2 г/кг, которую вводят за 5 ежедневных инфузий (400 мг/кг/введение) или за 2 ежедневных введения (1 г/кг/введение). При отсутствии эффекта от проводимой терапии или при исходно критически низком уровне тромбоцитов показано срочное введение отмытых материнских тромбоцитов [8].
При тяжелой тромбоцитопении обязательны также контроль за неврологическим статусом новорожденного, проведение нейросонографии и осмотр глазного дна в динамике. В тех случаях, когда количество тромбоцитов снижается до 50х109/л и ниже, а геморрагический синдром прогрессирует, показано назначение ИГВВ. Доказано, что терапевтический эффект ИГВВ достигается при курсовой дозе 2 г/кг, которую вводят за 5 ежедневных инфузий (400 мг/кг/введение) или за 2 ежедневных введения (1 г/кг/введение). При отсутствии эффекта от проводимой терапии или при исходно критически низком уровне тромбоцитов показано срочное введение отмытых материнских тромбоцитов [8].
Представленное клиническое наблюдение свидетельствует о том, что при развитии тромбоцитопении у новорожденного ребенка необходимо проводить дифференциальную диагностику с целым рядом патологических состояний. При этом нельзя забывать о том, что в основе неонатальных тромбоцитопений могут лежать иммунные механизмы, а их своевременная верификация позволит избежать диагностических ошибок и неадекватного лечения.
.
Лекарственно-индуцированная тромбоцитопения. Клиническая фармакология и терапия
Тромбоцитопения – это патологическое состояние, характеризующееся снижением числа тромбоцитов <150 × 109/л или >50% от исходного количества [1]. Тромбоцитопению считают средне-тяжелой, если число тромбоцитов находится в пределах 20-150 × 109л , и тяжелой, если оно снижается менее 20 × 109/л [2]. У пациентов с тяжелой тромбоцитопенией имеется высокий риск развития кровотечения, которое может привести к летальному исходу [3].
В 1998 году N. George и соавт. опубликовали обширный список лекарственных средств (ЛС), вызывающих тромбоцитопению [4], который постоянно обновляется и дополняется [5]. Классы ЛС, лечение которыми может сопровождаться тромбоцитопенией, включают в себя хинины, антимикробные препараты, антиагреганты, нестероидные противовоспалительные препараты (НПВП), антиконвульсанты, анальгетики, гепарин, химиотерапевтические ЛС, иммунодепрессанты и др. (табл. 1) [6].
(табл. 1) [6].
| Класс ЛС | Препараты | Частота | Уровень доказанности |
|---|---|---|---|
| Примечание: A — данные одного или нескольких рандомизированных контролируемых клинических исследований; уровень B — данные проспективных наблюдательных исследований, когортных исследований, ретроспективных исследований, исследований случай-контроль и/или постмаркетинговых исследований; C — описания клинических случаях или серии клинических случаев. *После первого (повторного) введения | |||
| Антибиотики | Антибиотики | 21% | C |
| Сульфасалазин | <1% | C | |
| Ванкомицин | Неизвестно | A | |
| Тримоксазол, сульфизоксазол, сульфатиазол, сульфаметоксазол, сульфизоксазол, бензилпенициллин, метициллин,ампициллин, феноксиметилпенициллин, цефтриаксон, цефуроксим, ципрофлоксацин, дактиномицин, налидиксовая кислот |
Неизвестно | C | |
| Другие антибактериальные ЛС (противотуберкулезные) | Аминосалициловая кислота, этамбутол, изониазид, рифампицин, нитрофурантоин | Неизвестно | C |
| Ингибиторы АПФ | Каптоприл, периндоприл | Неизвестно | C |
| Антиагреганты | Абциксимаб, эптифибатид | 0,5-1% (10-14%)* | A |
| Тирофибан | 0,2-0,5% | A | |
| Пентоксифиллин, клопидогрел | Неизвестно | C | |
| Антикоагулянты | Гепарин | 3-6% | А |
| Альфа-адреноблокаторы | Алфузозин, теразозин | Неизвестно | C |
| Альфа-адреномиметики | Метилдопа, нафазолин | Неизвестно | C |
| Бета-адреноблокаторы | Окспренолол, алпренолол | Неизвестно | C |
| Антиаритмические средства | Прокаинамид | 1% | C |
| Хинидин | <1% | C | |
| Амиодарон, фенитоин, дифенин | Неизвестно | C | |
| Анткагонисты кальция | Амлодипин | Неизвестно | C |
| Диуретики | Хлоротиазид, гидрохлоротиазид, спиронолактон, фуросемид, индапамид | Неизвестно | C |
| Сердечные гликозиды | Дигоксин, дигитоксин | Неизвестно | А/C |
| Вазодилататоры | Диазоксид, миноксидил | Неизвестно | C |
| Фибраты | Фенофибрат | Неизвестно | C |
| Статины | Симвастатин | <0,1% | C |
| Нитраты | Нитроглицерин | Неизвестно | C |
| НПВП | |||
Произв. уксусной к-ты уксусной к-ты |
Диклофенак, сулиндак, толметин | <1% | C |
| Произв. пропионовой к-ты | Ибупрофен, напроксен | <1% | C |
| Оксикамы | Мелоксикам | Неизвестно | C |
| Произв. салициловой к-ты | Ацетилсалициловая кислота | Неизвестно | C |
| Бутиллпиразолидины | Оксифенбутазон | Неизвестно | C |
| Противовирусные средства | Адефовира дипивоксил, интерферон альфа, лопинавир + ритонавир | Неизвестно | C |
| Антигельминтные средств | Левамизол | Неизвестно | C |
| Анксиолитики | Диазепам, лоразепам | Неизвестно | C |
| Антипсихотики | Хлорпромазин, галоперидол, тиотиксен, кветиапин, мелперон, рисперидон | Неизвестно | C |
| Противоэпилептические ЛС | Вальпроат натрия | 20% | C |
| Карбамазепин, фенитоин, дифенин, ламотриджин, леветирацетам | Неизвестно | C | |
| Противоопухлевые средства | Тамоксифен, бортезомиб, ритуксимаб, иринотекан | Неизвестно | C |
| Иммунодепрессанты | Эфализумаб | 0,3% | А |
| Противомалярийные | Хинин | <1% | C |
| противопротозойные средства | Стибофен, метронидазол, пентостам | Неизвестно | C |
| Простагландины | Илопрост | Неизвестно | C |
| Детоксицирующие ЛС | Дефероксамин | Неизвестно | C |
| Гормоны | Даназол, октреотид, глюкагон | Неизвестно | C |
| H2-блокаторы | Циметидин, фамотидин, ранитидин | Неизвестно | C |
| Гипогликемические препараты | Хлорпропамид, глибенкламид | Неизвестно | C |
| Ингибиторы синтеза стероидов |
Аминоглютетимид | Неизвестно | C |
| Анилиды | Ацетаминофен | Неизвестно | C |
| Соли золота | Ридаура, солганал | Неизвестно | C |
| Дерматотропные средства | Изотретиноин | Неизвестно | C |
| Вакцины | Гепатит В, грипп, пневмококк, полиомиелит | Неизвестно | C |
| Стабилизаторы мембран тучных клеток |
Траниласт | Неизвестно | C |
| Витамины | В12 | Неизвестно | С |
Эпидемиология
Хотя тромбоцитопения является побочным эффектом многих ЛС, она наблюдается все же редко. Точная частота лекарственноиндуцированной тромбоцитопении неизве ст на, но приблизительно составляет 10 случаев на 1 млн человек в год [3,6]. Риск развития тромбоцитопении варьируется в широких пределах и зависит от конкретного препарата. Например, при лечении триметопримом/сульфаметоксазолом (ко-тримоксазолом) риск тромбоцитопении достигает 38 случаев на 1 млн пациентов, а при приеме хинина или хинидина – 26 случаев на 1 млн пациентов [6].
Точная частота лекарственноиндуцированной тромбоцитопении неизве ст на, но приблизительно составляет 10 случаев на 1 млн человек в год [3,6]. Риск развития тромбоцитопении варьируется в широких пределах и зависит от конкретного препарата. Например, при лечении триметопримом/сульфаметоксазолом (ко-тримоксазолом) риск тромбоцитопении достигает 38 случаев на 1 млн пациентов, а при приеме хинина или хинидина – 26 случаев на 1 млн пациентов [6].
Механизмы развития тромбоцитопении
Выделяют иммунологические и неиммунологические механизмы развития лекарственно-индуцированной тромбоцитопении (табл. 2).
| Лекарственные средства | Механизм |
|---|---|
| Абциксимаб, эптифибатид, тирофибан | Лекарственно-зависимое распознавание Fab фрагмента и неоэпитопа ГПIIb/IIIa |
| Хлорамфеникол, линезолид | Нарушение митохондриального дыхания |
| Соли золота, прокаинамид | Аутоантитела |
| Гепарин, низкомолекулярный гепарин | Антитела, направленные против эпитопа, сформированного комплексом гепарина и ФТ4 |
| Хинин, хинидин, сульфаниламиды, НПВП, ацетаминофен (парацетамол) |
Образование сложного эпитопа |
| Вальпроевая кислота, амиодарон | Неидиосинкразический дозо-зависимый |
| Ванкомицин | Ванкомицин-зависимые антитела против ГП IIb/IIIa |
Лекарственные средства как гаптены. Образование ковалентных связей между молекулами лекарственного средства (гаптенами) и собственными белками организма человека может привести к образованию специфических антител к фомирующемуся комплексу [7-9]. В настоящее время убедительно не доказано, что этот механизм играет центральную роль в развитии лекарственно-индуцированной тромбоцитопении, за исключением тромбоцитопении, вызванной пенициллином [10]. Как правило, антитела не направлены исключительно против ЛС (гаптена), ковалентно присоединенного к тромбоцитам, и способны перекрестно взаимодействать с тромбоцитами, вызывая тем самым тромбоцитопению [11].
Образование ковалентных связей между молекулами лекарственного средства (гаптенами) и собственными белками организма человека может привести к образованию специфических антител к фомирующемуся комплексу [7-9]. В настоящее время убедительно не доказано, что этот механизм играет центральную роль в развитии лекарственно-индуцированной тромбоцитопении, за исключением тромбоцитопении, вызванной пенициллином [10]. Как правило, антитела не направлены исключительно против ЛС (гаптена), ковалентно присоединенного к тромбоцитам, и способны перекрестно взаимодействать с тромбоцитами, вызывая тем самым тромбоцитопению [11].
Формирование эпитопа. Хинин, хинидин, судьфаниламиды, НПВП и их метаболиты вызывают тромбоцитопению, формируя новый эпитоп (часть ЛС, белка) [6,12]. Хинин используется для лечения малярии, а также входит в состав напитков, которые могут употребляться в комбинации с алкоголем. Также хинин применяется для лечения так называемых ночных крапми (периодически возникающих судорог ног, сопровождающиеся болезненными ощущениями, которые относятся к расстройствам движений во сне), хотя это показание не одобрено Американской администрацией по контролю за пищевыми продуктами и лекарствами (FDA) из-за риска развития побочных эффектов [13]. Считается что хинин вызывает структурные модификации гликопротеина (ГП) тромбоцитов посредством двух возможных механизмов. Первый механизм заключается во взаимодействии хинина с ГП с образованием комплементарных связей с последующей модификацией гидрофильных и/или гидрофобных доменов [6,14]. Вырабатываемые антитела могут взаимодействовать с ЛС, фиксированными на тромбоцитах, а также с белковыми структурами последних, которые непосредственно контактируют с ЛС, что приводит к деструкции тромбоцитов [11]. Второй широко обсуждаемый потенциальный механизм состоит в том, что ЛС, связываясь с одним участком ГП, может вызывать структурные модификации в другом его локусе и потенцировать распознавание такой измененной области соответствующим антителом с последующим лизисом [11]. Известно, что участок связывания с антигеном (Fab) в структуре антитела служит той областью, посредством которой ЛС может опосредовать взаимодействие антитела с тем или иным антигеном [15]. Мишенью таких антител являются эпитопы комплексов ГП IIb/3a или ГП Ib/V/IX [10,14,16].
Считается что хинин вызывает структурные модификации гликопротеина (ГП) тромбоцитов посредством двух возможных механизмов. Первый механизм заключается во взаимодействии хинина с ГП с образованием комплементарных связей с последующей модификацией гидрофильных и/или гидрофобных доменов [6,14]. Вырабатываемые антитела могут взаимодействовать с ЛС, фиксированными на тромбоцитах, а также с белковыми структурами последних, которые непосредственно контактируют с ЛС, что приводит к деструкции тромбоцитов [11]. Второй широко обсуждаемый потенциальный механизм состоит в том, что ЛС, связываясь с одним участком ГП, может вызывать структурные модификации в другом его локусе и потенцировать распознавание такой измененной области соответствующим антителом с последующим лизисом [11]. Известно, что участок связывания с антигеном (Fab) в структуре антитела служит той областью, посредством которой ЛС может опосредовать взаимодействие антитела с тем или иным антигеном [15]. Мишенью таких антител являются эпитопы комплексов ГП IIb/3a или ГП Ib/V/IX [10,14,16].
Лекарственно-индуцированные аутоантитела. Ауто ан титела в редких случаях способны разрушать тромбоциты после воздействия ЛС, например, у пациентов с ревматоидным артритом, получающих терапию солями золота (в 1-3% случаев). Золото-индуцированная тромбоцитопения может развиться сразу или спустя некоторое время после воздействия данных ЛС [17]. Количества тромбоцитов снижается очень быстро или постепенно – в течение нескольких недель или месяцев Отсроченное начало тромбоцитопении может ассоциироваться с панцитопенией. Остро возникшая тромбоцитопения при применении препаратов золота может протекать по типу идиопатической тромбоцитопенической пурпуры (ТТП), при которой происходит иммуноопосредованное разрушение тромбоцитов в крови, однако в костном мозге формируются неизмененные мегакариоциты, что подтверждается данными биопсии [17]. Золото стимулирует процесс связывания иммуно глобулина G с ГП V, расположенным на поверхности тромбоцита. Механизм данного взаимодействия неизвестен [10,18]. Эта аутоиммунная реакция не зависит от концентрации солей золота и может наблюдаться даже после отмены препарата [18]. Сходный механизм был описан при использовании прокаинамида, но целевой ГП определен не был [19,20].
Эта аутоиммунная реакция не зависит от концентрации солей золота и может наблюдаться даже после отмены препарата [18]. Сходный механизм был описан при использовании прокаинамида, но целевой ГП определен не был [19,20].
Гепарин-индуцированная тромбоцитопения. Выделяют два типа гепарин-индуцированной тромбоцитопении (ГИТ). ГИТ первого типа не связана с иммунными механизмами и носит доброкачественный характер, в то время как ГИТ второго типа возникает в результате взаимодействия антител с комплексом гепарина и 4 фактора тромбоцитов (ФТ4) [21,22]. ФТ4 – это цитокин, содержащийся в альфа гранулах тромбоцитов и выделяющийся при их агрегации. Считается что ФТ4 участвует в процессах коагуляции, воспаления и хемотаксиса и выделяется у 1-3% пациентов, принимающих гепарин [22]. Гепарин образует комплекс с ФТ4, а антитела распознают его как новый эпитоп [22-24]. Гепарин может также вызвать конформационные изменения структуры ФТ4 [22]. Ведущую роль в патогенезе ГИТ играют IgG и в меньшей степени IgA и IgM [22,24]. Антитела к комплексу гепарин-ФТ4 обнаруживают не только у пациентов с ГИТ, но и пациентов без тромбоцитопении [22]. В редких случаях число тромбоцитов при ГИТ снижается <10 × 109/л [25]. ГИТ обычно развивается через 5-10 дней после начала лечения [26]. В отличие от остальных типов лекарственно-индуцированной тромбоцитопении, при ГИТ имеется высокий риск тромбоэмболических осложнений [21,22,27]. Низкомолекулярные гепарины (НМГ), такие как эноксапарин и далтепарин, также могут вызвать ГИТ, в то как при применении фондапаринукса, ингибирующего фактор Ха, риск ее развития низкий.
Антитела к комплексу гепарин-ФТ4 обнаруживают не только у пациентов с ГИТ, но и пациентов без тромбоцитопении [22]. В редких случаях число тромбоцитов при ГИТ снижается <10 × 109/л [25]. ГИТ обычно развивается через 5-10 дней после начала лечения [26]. В отличие от остальных типов лекарственно-индуцированной тромбоцитопении, при ГИТ имеется высокий риск тромбоэмболических осложнений [21,22,27]. Низкомолекулярные гепарины (НМГ), такие как эноксапарин и далтепарин, также могут вызвать ГИТ, в то как при применении фондапаринукса, ингибирующего фактор Ха, риск ее развития низкий.
Блокаторы ГП IIb/IIIa. Абциксимаб, тирофибан и эптифибатид ингибируют гликопротеиновый комплекс IIb/IIIa тромбоцитов (ГП IIb/IIIa) и взаимодействие с ним фибриногена и тем сам подавляют тромбообразование [30]. Применяются для профилактики рестеноза после чрескожной транслюминальной коронарной ангиопластики [31-34]. Блокаторы ГП IIb/IIIa вызывают тромбоцитопению в течение часа после введения примерно у 1% пациентов, при повторном введении – у 4% [32-34]. Абциксимаб – это химерный Fab фрагмент, синтезируемый из мышиных моноклональных антител 7Е3. Острая тромбоцитопения, характеризующаяся резким снижением числа тромбоцитов в течение часа после введения препарата, объясняется образованием антител к компонентам абциксимаба [6,34]. По сравнению с другими препаратами этой группы абциксимаб вызывает более тяжелую тромбоцитопению со снижением количества тромбоцитов до <10 × 109/л . Может также наблюдаться отсроченная тромбоцитопения спустя неделю после введения ЛC, по-видимому, за счет вновь синтезируемых IgG и IgM, которые распознают эпитопы комплекса абциксимаб-тромбоцит [32,34]. Некоторые факторы ассоциируются с увеличением риска развития тромбоцитопении у пациентов, получающих ингибиторы фибриногена, включая сочетанное применение ацетилсалициловой кислоты или гепарина, внутриаортальную баллонную контрпульсацию [35,36].
Абциксимаб – это химерный Fab фрагмент, синтезируемый из мышиных моноклональных антител 7Е3. Острая тромбоцитопения, характеризующаяся резким снижением числа тромбоцитов в течение часа после введения препарата, объясняется образованием антител к компонентам абциксимаба [6,34]. По сравнению с другими препаратами этой группы абциксимаб вызывает более тяжелую тромбоцитопению со снижением количества тромбоцитов до <10 × 109/л . Может также наблюдаться отсроченная тромбоцитопения спустя неделю после введения ЛC, по-видимому, за счет вновь синтезируемых IgG и IgM, которые распознают эпитопы комплекса абциксимаб-тромбоцит [32,34]. Некоторые факторы ассоциируются с увеличением риска развития тромбоцитопении у пациентов, получающих ингибиторы фибриногена, включая сочетанное применение ацетилсалициловой кислоты или гепарина, внутриаортальную баллонную контрпульсацию [35,36].
Тирофибан и эптифибатид взаимодействуют на ГПIIb/IIIa с сайтом связывания аминокислотного фрагмента аргинин-глицин-аспарагиновая кислота и тем самым служат антагонистами связывания фибриногена и, соответственно, агрегации тромбоцитов [31].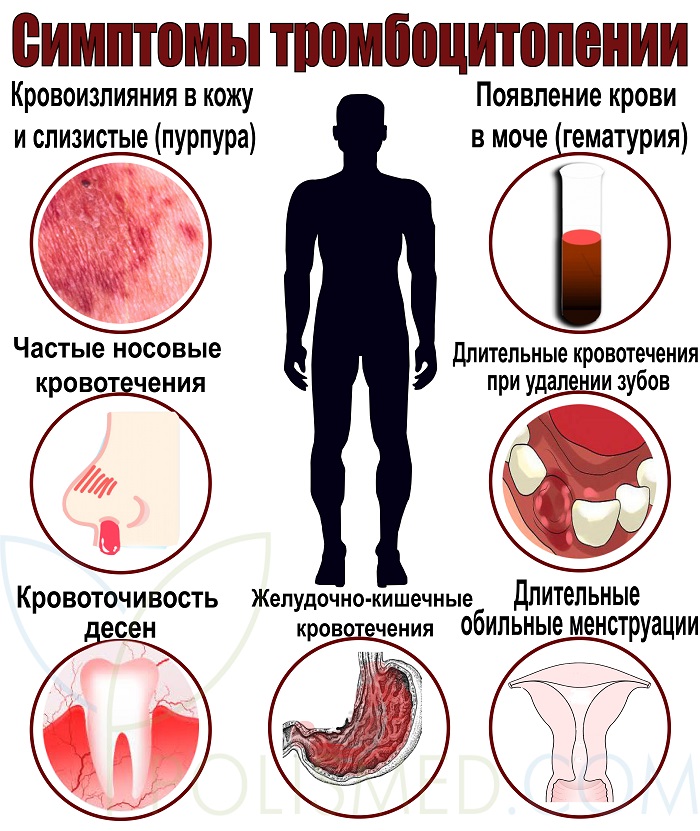 Лекарственно-зависимые антитела могут распознавать несколько эпитопов благодаря конформационным изменениям, присущим тирофибану и эптифибатиду [31,33]. Как возможные причины тромбоцитопении рассматриваются и другие механизмы, не связанные с аутоиммунными реакциями, однако точный механизм ее развития остается неизвестным [31].
Лекарственно-зависимые антитела могут распознавать несколько эпитопов благодаря конформационным изменениям, присущим тирофибану и эптифибатиду [31,33]. Как возможные причины тромбоцитопении рассматриваются и другие механизмы, не связанные с аутоиммунными реакциями, однако точный механизм ее развития остается неизвестным [31].
Блокаторы h3-гистаминовых рецепторов. Также могут выступать в качестве триггеров тромбоцитопении [37]. Наибольшее количество случаев зарегистрировано в отделениях интенсивной терапии, где данные ЛС используются для лечения стрессовых язв верхних отделов желудочно-кишечного тракта. Предполагаемые механизмы включают супрессию костного мозга посредством ингибирования дифференцировки стволовых клеток и образование IgG антител к компонентам самого костного мозга [37]. Однако в ряде ретроспективных и проспективных исследованиях не было получено убедительных доказательств роли блокаторов h3-гистаминовых в развитии тромбоцитопении [38,39].
Тромботическая тромбоцитопеническая пурпура. ТТП и гемолитико-уремический синдром (ГУС). Термины, используемые для описания целого ряда клинических состояний, характеризующихся микрососудистой гемолитической анемией, фрагментацией эритроцитов (шистоцитоз), тромбоцитопенией и другими клиническими проявлениями и сопровождающихся очень высокой летальностью (до 90%) [40,41]. Возможны осложнения с развитием почечной недостаточности, неврологической симптоматики, лихорадки и кровотечения. ТТП и ГУС могут развиться в результате дефицита протеаз, разрушающих фактор фон Виллебранда, инфекции, вызванной E. coli O157:H7, трансплантации гемопоэтических стволовых клеток и воздействии некоторых ЛС [40,42-44]. Имеются данные о лекарствен ноиндуцированных ТТП и ГУС при воздействия митомицина С, циклоспорина, такролимуса, сиролимуса, хинина, тиклопидина, клопидогрела и симвастатина [40,41,45-50)]. Лекарственно-индуцированная ТТП возникает в результате повреждения эндотелиальных клеток и приводит к развитию тромботической микроангиопатии. Данный механизм наблюдается при применении митомицина С, такролимуса, сиролимуса и циклоспорина [41,48]. Важно отметить, что эти препараты вызывают дозозависимую ТТП [41]. Напротив, хинин-индуцированная ТТП возникает в результате образования антител к растворимой форме ЛС [45]. Хинин-индуцированная ТТП, ассоциированная с образованием антител, может развиться после однократного или непродолжительного приема хинина [41,43,45]. Тиклопидин и клопидогрел-индуцированная ТТП является парадоксальной (антиагреганты в некоторых случаях дают прямо противолположный эффект, способствуя формированию тромбов). Механизм ее остается неизвестным [42,44,45,47,49,50)]. Частота ТТП при назначении данных препаратов составляет <1% и соответствует таковой в общей популяции [41].
Данный механизм наблюдается при применении митомицина С, такролимуса, сиролимуса и циклоспорина [41,48]. Важно отметить, что эти препараты вызывают дозозависимую ТТП [41]. Напротив, хинин-индуцированная ТТП возникает в результате образования антител к растворимой форме ЛС [45]. Хинин-индуцированная ТТП, ассоциированная с образованием антител, может развиться после однократного или непродолжительного приема хинина [41,43,45]. Тиклопидин и клопидогрел-индуцированная ТТП является парадоксальной (антиагреганты в некоторых случаях дают прямо противолположный эффект, способствуя формированию тромбов). Механизм ее остается неизвестным [42,44,45,47,49,50)]. Частота ТТП при назначении данных препаратов составляет <1% и соответствует таковой в общей популяции [41].
Этилендиаминтетрауксусная кислота (ЭДТА). Яв ля ется кальций-хелатным антикоагулянтом, используемым in vitro. ЭДТА способна взаимодействовать in vitro с аутоантителами, направленными против ГПIIb/IIIa, в результате чего в образцах крови возникает разрушение тромбоцитов. При этом на этапе исследования крови в лабораторном цитометрическом оборудовании может создаватся ложное суждение о наличии тромбоцитопении [51]. Такого рода тромбоцитопения наблюдается приблизительно в 0,1% случаев. Ее можно избежать, используя в качестве антикоагулянта цитрат натрия или гепарин.
При этом на этапе исследования крови в лабораторном цитометрическом оборудовании может создаватся ложное суждение о наличии тромбоцитопении [51]. Такого рода тромбоцитопения наблюдается приблизительно в 0,1% случаев. Ее можно избежать, используя в качестве антикоагулянта цитрат натрия или гепарин.
Клиническая картина, лабораторная диагностика и дифференциальный диагноз
Лекарственно-индуцированная тромбоцитопения обычно развивается в течение 1-2 недель после приема ЛС, однако симптомы могут возникнуть и непосредственно после введения препарата (табл. 3). У пациентов наблюдаются петехии, экхимозы и пурпура, а также носовое кровотечение, гематурия, кровоточивость десен и гематохезия. Риск развития кровотечений у пациентов с лекарственно-индуцированной тромбоцитопенией, не ассоциированной с приемом гепарина, составляет в среднем 9%, а связанная с ним смертность – 0,8% [4,5]. У половины пациентов с ГИТ наблюдают развитие тромботических осложнений [56], причем венозные тромбозы, в частности тромбоэмболия легочной артерии, встречаются чаще артериальных. Риск возникновения тромботических осложнений сохраняется в течение несколько недель после восстановления количества тромбоцитов [56]. ТТП ассоциируется с развитием инсульта, инфаркта миокарда и почечной недостаточности. При отсутствии лечения смертность пациентов с ТТП составляет около 90% [40,41]. Считается, что плазмаферез при хинин-индуцированной ТТП увеличивает выживаемость с 25% до 100% [49], однако неврологические симптомы и почечная недостаточность могут сохраняться после лечения [45].
Риск возникновения тромботических осложнений сохраняется в течение несколько недель после восстановления количества тромбоцитов [56]. ТТП ассоциируется с развитием инсульта, инфаркта миокарда и почечной недостаточности. При отсутствии лечения смертность пациентов с ТТП составляет около 90% [40,41]. Считается, что плазмаферез при хинин-индуцированной ТТП увеличивает выживаемость с 25% до 100% [49], однако неврологические симптомы и почечная недостаточность могут сохраняться после лечения [45].
| Общие проявления | Тромбоцитопения средней степени тяжести |
Тяжелая тромбоцитопения | ГИТ – специфические симптомы |
|---|---|---|---|
| Озноб, головокружение, усталость, лихорадка, тошнота, рвота |
Экхимозы, микрогематурия, петехии, пурпура |
Носовое кровотечение, пурпура кровоточивость десен, макрогематурия, кровянистый стул, меноррагия, забрюшинное кровотечение |
Анафилаксия, гангрена, некроз кожи, тромбоз глубоких вен конечностей, тромбоэмболия легочной артерии |
Поскольку ГИТ в прогностическом плане является неблагоприятным состоянием и представляет собой одну из важнейших проблем в сфере интервенционной кардиологии и интенсивной терапии пациентов кардиологического профиля, то актуальным является внедрение в клиническую практику стандартизированной системы оценки риска возникновения ГИТ. Для характеристики признаков ГИТ может быть использована шкала 4Т: (1) относительное снижение количества тромбоцитов; (2) время начала снижения количества тромбоцитов; (3) наличие или отсутствие тромбоза; (4) другие причины. Каждый пункт оценивается в баллах от 0 до 2. Чем больше сумма баллов, тем выше риск возникновения ГИТ [22].
Для характеристики признаков ГИТ может быть использована шкала 4Т: (1) относительное снижение количества тромбоцитов; (2) время начала снижения количества тромбоцитов; (3) наличие или отсутствие тромбоза; (4) другие причины. Каждый пункт оценивается в баллах от 0 до 2. Чем больше сумма баллов, тем выше риск возникновения ГИТ [22].
Большое значение в ранней диагностике лекарственно-индуцированной тромбоцитопении имеет информированность пациента, который(ая) должен(на) обращать внимание на необычные кровоподтеки, обильные или длительные менструации, длительное кровотечение из десен после чистки зубов или зубной нитью и продолжительное кровотечение из незначительного пореза. В таких случаях следует немедленно связаться со своим лечащим врачом.
Дифференциальный диагноз между снижением продукции тромбоцитов, увеличением деструкции тромбоцитов, секвестрацией тромбоцитов селезенкой или гемодилюцией, как правило, проводится с учетом результатов общего анализа крови, включая количество тромбоцитов и гематокрит, исследования селезенки и данных трепанобиопсии костного мозга. Резкое снижение количества тромбоцитов может указывать на их массивное разрушение различного генеза. Снижение числа мегакариоцитов в биоптате костного мозга и наличие панцитопении свидетельствует о развитии тромбоцитопении по гипопродуктивному типу. Спленомегалия может приводить к развитию тромбоцитопении на фоне перераспределения кровотока в сосудистых бассейнах селезенки. Гемодилюция может быть результатом введения растворов коллоидов, кристаллоидов или продуктов тромбоцитов, что приводит к относительной тромбоцитопении. Следует учитывать, что тромбоцитопения, развивающаяся на фоне терапии ЛС, которые могут вызывать снижение количества тромбоцитов крови, не всегда связана именно с приемом подобных препаратов.
Резкое снижение количества тромбоцитов может указывать на их массивное разрушение различного генеза. Снижение числа мегакариоцитов в биоптате костного мозга и наличие панцитопении свидетельствует о развитии тромбоцитопении по гипопродуктивному типу. Спленомегалия может приводить к развитию тромбоцитопении на фоне перераспределения кровотока в сосудистых бассейнах селезенки. Гемодилюция может быть результатом введения растворов коллоидов, кристаллоидов или продуктов тромбоцитов, что приводит к относительной тромбоцитопении. Следует учитывать, что тромбоцитопения, развивающаяся на фоне терапии ЛС, которые могут вызывать снижение количества тромбоцитов крови, не всегда связана именно с приемом подобных препаратов.
Лекарственно-индуцированная тромбоцитопения чаще является диагнозом исключения. Список для дифференциального диагноза обширен и включает такие заболевания, как острый лимфоидный лейкоз, острый миелолейкоз, апластическую анемию, хроническую печеночную недостаточность, хронический лейкоз, нарушение кроветворения, синдром диссеминированного внутрисосудистого свертывания, заболевания печени, ВИЧ-инфекцию, иммунную (идиопатическую) тромбоцитопеническую пурпуру, введение катетера в легочные артерии, лимфомы, метастазы, миелодиспластический синдром, миелопролиферативные синдромы, беременность, протезирование клапанов, псевдотромбоцитопению, сепсис, спленомегалию, васкулиты [22, 34,52].
Лабораторное подтверждение лекарственно-индуцированной тромбоцитопении вызывает большие слож ности из-за отсутствия лекарственно-зависимых антитромбоцитарных антител для тестирования. Необходимо тщательно оценить данные истории болезни пациента с тромбоцитопенией, чтобы определить все возможные причины ее развития, в том числе связь с лекарственной терапией. Лабораторные исследования при лекарственно-индуцированной тромбоцитопении могут включать определение ГП-специфических антител к тромбоцитам и лекарственно-индуцированного увеличения тромбоцит-ассоциированного IgG [52]. При ГИТ определяют секрецию тромбоцитами C-серотонина или антитела к комплексу ФТ4-гепарин. Прог нос тическая ценность положительных результатов данных анализов составляет 89-100% и 10-93%, соответственно [21,52], а прогностическая ценность отрицательных результатов – 80% и 95%, [21].
Факторы риска
Факторы риска развития лекарственно-индуцированной тромбоцитопении отличаются при применении разных ЛС [53]. Так, риск развития тромбоцитопении зависит от концентрации в плазме такролимуса, циклоспорина, сиролимуса и вальпроевой кислоты [41,48]. Риск развития лекарственно-индуцированной тромбоцитопении на фоне применения вальпроевой кислоты увеличивается при использовании ее в дозе более 1000 мг/сут, сопутствующем применении ацетилсалициловой кислоты, а также у пациентов старческого возраста [54]. Риск развития лекарственно-индуцированной тромбоцитопении при лечении линезолидом ассоциируется с длительностью терапии (более 2
Так, риск развития тромбоцитопении зависит от концентрации в плазме такролимуса, циклоспорина, сиролимуса и вальпроевой кислоты [41,48]. Риск развития лекарственно-индуцированной тромбоцитопении на фоне применения вальпроевой кислоты увеличивается при использовании ее в дозе более 1000 мг/сут, сопутствующем применении ацетилсалициловой кислоты, а также у пациентов старческого возраста [54]. Риск развития лекарственно-индуцированной тромбоцитопении при лечении линезолидом ассоциируется с длительностью терапии (более 2
недель) [55]. Риск развития лекарственно-индуцированной тромбоцитопении на фоне использования гепарина или НМГ увеличивается при наличии в анамнезе ГИТ и предшествующем (особенно в течение предыдущих 100 дней) использовании этих препаратов [56]. У паци ентов, получающих ингибиторы фибриногена, вероятность развития тромбоцитопении выше при одновременном применении ацетилсалициловой кислоты или гепарина, а также при проведении внутриаортальной баллонной контрпульсации [35,36].
Профилактика и лечение
Многие часто назначаемые препараты могут вызывать лекарственно-индуцированную тромбоцитопению, поэтому ее профилактика является сложной задачей. В отличие от тромбоцитопении, ассоциированной с приемом многих других ЛС, тромбоцитопения, вызванная химиотерапевтическими препаратами, предсказуема, что позволяет избежать резкого снижения числа тромбоцитов в крови путем коррекции доз ЛС. Для лечения тяжелой тромбоцитопении, развивающейся на фоне химиотерапии, может быть использован опрелвекин (интерлейкин-11), который способствует росту и дифференцировке мегакариоцитов [57,58]. Его назначают в дозе 50 мкг/кг один раз в сутки подкожно спустя 6-24 часа после завершения химиотерапии (не более 21 дня). Терапия препаратом должна быть прекращена, как минимум, за два дня до очередного курса химиотерапии. В Российской Федерации этот препарат не зарегистрирован.
В случае развития лекарственно-индуцированной тромбоцитопении необходимо прекратить прием ЛС, предположительно вызывающего тромбоцитопению. В большинстве случаев количество тромбоцитов возвращается к исходному уровню относительно быстро – в среднем в течение 7 дней (от 1 до 30 дней) [3].
В большинстве случаев количество тромбоцитов возвращается к исходному уровню относительно быстро – в среднем в течение 7 дней (от 1 до 30 дней) [3].
У всех пациентов, получающих нефракционированный гепарин или НМГ, необходимо контролировать количество тромбоцитов в крови на 4-й и 14-й день терапии. Главная цель лечения ГИТ – предотвратить развитие тромботических осложнений путем снижения активации тромбоцитов и тромбина с помощью прямых ингибиторов тромбина (лепирудин, бивалирудин и аргатробан) или гепариноидов (анапароид) [21,59]. НМГ не следует назначать пациентам с ГИТ, учитывая высокую перекрестную реактивность с ФТ4 и антителами к гепарину [22,59]. Назначение варфарина возможно после разрешения тромбоцитопении, т.е. увеличения их количества >150000 × 109/л). Если симптомы ГИТ не сохраняются до начала терапии варфарином, то может возникнуть молниеносная венозная гангрена конечности [22,52,60,61]. Прямые ингибиторы тромбина непосредственно связывают и инактивируют тромбин без участия антитромбина. Перекрестная реактивность между гепарином и прямыми ингибиторами тромбина отсутствует. Прямые ингибиторы тромбина и гепариноиды имеют короткий период полувыведения (25-80 мин) [22,56].
Перекрестная реактивность между гепарином и прямыми ингибиторами тромбина отсутствует. Прямые ингибиторы тромбина и гепариноиды имеют короткий период полувыведения (25-80 мин) [22,56].
Лепирудин представляет собой рекомбинантное производное гирудина (т.е. белка пиявок). Препарат одобрен FDA для лечения ГИТ и связанных с ней тромбоэмболических осложнений. В опасных для жизни ситуациях возможно введение болюсной дозы 0,2 мг/кг. Рекомендуемая скорость инфузии составляет 0,10 мг/кг/ч. Активированное частичное тромбопластиновое время (АЧТВ) следует измерять каждые 4 часа, а затем каждые 4-5 периодов полувыведения ЛС [22,59]. Во многих исследованиях лечение лепирудином у пациентов с ГИТ приводило к снижению смертности, частоты тромбозов и ампутаций конечностей [62-64], но ассоциировалось с увеличением частоты кровотечений. Опубликованы сообщения об образовании антител к лепиридину при его повторном введении, а также после введения даже одной болюсной дозы, которое сопровождалось фатальными анафилактическими реакциями [64,65]. В связи с этим повторное введение препарата не рекомендуется.
В связи с этим повторное введение препарата не рекомендуется.
Бивалирудин является синтетическим ингибитором тромбина и одобрен для применения при чрескожном коронарном вмешательстве у пациентов с ГИТ или повышенным риском ее развития [21]. Период полувыведения бивалирудина короче, чем лепирудина (25 и 80 мин, соответственно). Препарат подвергается фер ментативному метаболизму, поэтому у пациентов с почечной недостаточностью необходима лишь незначительные коррекция дозы [21,22,52]. При лечении ГИТ требуется болюсная доза, начальная скорость инфузии составляет от 0,15 до 0,2 мг/кг/ч, а при наличии почечной недостаточности – 0,03-0,1 мг/кг/ч. Необходимо контролировать АЧТВ, которое должно быть в 1,5-2,5 раза выше по сравнению с исходным уровнем [54,55].
Аргатробан также является прямым ингибитором тромбина [66] и используется для лечения и профилактики тромбозов у пациентов с ГИТ. Болюсная доза не требуется, а начальная скорость инфузии составляет 2 мкг/кг/мин. Для достижения целевых уровней АЧТВ дозы могут варьироваться от 0,5 до 2 мкг/кг/мин. В отличие от других прямых ингибиторов тромбина, аргатробан метаболизируется в печени. У пациентов с печеночной недостаточностью (7-11 баллов по шкале Чайлд-Пью) дозу следует уменьшить до 0,5 мкг/кг/мин. Препарат противопоказан пациентам с повышенной активностью аминотрансфераз более чем в 3 раза по сравнению с верхней границей нормы [67-69]. АЧТВ следует поддерживать на уровне в 1,5-3 раза выше нормы. В клинических исследованиях у пациентов с ГИТ лечение аргатробаном приводило к снижению частоты тромботических осложнений [22,68,69].
Для достижения целевых уровней АЧТВ дозы могут варьироваться от 0,5 до 2 мкг/кг/мин. В отличие от других прямых ингибиторов тромбина, аргатробан метаболизируется в печени. У пациентов с печеночной недостаточностью (7-11 баллов по шкале Чайлд-Пью) дозу следует уменьшить до 0,5 мкг/кг/мин. Препарат противопоказан пациентам с повышенной активностью аминотрансфераз более чем в 3 раза по сравнению с верхней границей нормы [67-69]. АЧТВ следует поддерживать на уровне в 1,5-3 раза выше нормы. В клинических исследованиях у пациентов с ГИТ лечение аргатробаном приводило к снижению частоты тромботических осложнений [22,68,69].
Для лечения ГИТ также используется данапароид, который относится к группе гепариноидов [70]. Механизм действия препарата заключается в ингибировании активации фактора X через антитромбин [71].
Опыт применения пероральных антикоагулянтов прямого действия у пациентов с ГИТ ограничивается отдельными клиническими случаями, что не позволяет рекомендовать их использование для лечения этого состояния [72].
Тромбоцитопения является хорошо известным побочным эффектом химиотерапии. В зависимости от режима химиотерапии и количества предыдущих циклов количество тромбоцитов обычно постепенно возвращается к норме [73]. Однако в определенных ситуациях может потребоваться трансфузия тромбоцитной массы [73-75]. Эксперты Американского общества клинических онкологов рекомендует проводить ее пациентам без признаков активного кровотечения, когда количество тромбоцитов снижается <10× 109/л [75]. При некоторых онкологических заболеваниях, таких как колоректальный рак, рак мочевого пузыря и меланома, трансфузия тромбоцитной массы возможна и при более высоком количестве тромбоцитов в крови [76]. Для безопасного оперативного вмешательства количество тромбоцитов должен быть не менее 40-50 × 109/л [77]. Трансфузия тромбоцитной массы может сопровождаться лихорадкой, аллергическими реакциями, аллоиммунизацией и инфекциями [73] и не рекомендуется пациентам с ГИТ [78].
Глюкокортикостероиды (ГКС), например, метилпреднизолон в дозе 1 мг/кг внутривенно каждые 8 ч или преднизолон в дозе до 1 мг/кг/сут внутрь, и высокие дозы внутривенного иммуноглобулина применяли для лечения лекарственно-индуцированной тромбоцитопении, хотя польза их убедительно не доказана [73,79]. Часто бывает трудно провести дифференциальный диагноз между иммунной ТТП и лекарственно-индуцируемой тромбоцитопенией. Поскольку ГКС оказались полезными при лечении иммунной ТТП, их рекомендуют использовать, по крайней мере, до тех пор, пока не будет исключен этот диагноз [3]. Пациентам с иммунной ТТП может быть также назначен внутривенный иммуноглобулин в дозе 1 г/кг/сут [80]. У пациентов с тромбоцитопенией изучалась эффективность ромипластина и элтромбопага, которые регулируют синтез мегакариоцитов и тромбоцитов [81-83], однако их польза при лекарственно-индуцированной тромбоцитопении не установлена. Эти препараты могут применяться при хронической иммунной ТТП [84].
Заключение
В случае развития тромбоцитопении необходимо помнить о возможной ее ассоциации с приемом ЛС. Целесообразно провести анализ всех лекарственных назначений и при необходимости скорректировать схему фармакотерапии.
ОСОБЕННОСТИ КЛИНИЧЕСКОЙ КАРТИНЫ И ОЦЕНКА ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ ИММУННЫХ ТРОМБОЦИТОПЕНИЙ У ДЕТЕЙ ИРКУТСКОЙ ОБЛАСТИ | Мартынович
1. Агеенкова Э.В., Петров В.Ю., Донюш Е.К., Со- сков Г.И. Эффективность применения внутривенного иммуноглобулина при иммунной тромбоцитопениче- ской пурпуре у детей // Инновационные технологии в педиатрии и детской хирургии: Матер. IX Рос. конгр. – М., 2010. – С. 324.
2. Баркаган Л.З. Нарушение гемостаза у детей. – М.: Медицина, 1991. – С. 58–111. Barkagan LZ. (1991).
3. Ефремов А.В. Геморрагические диатезы у де- тей. – М.: ГОУ ВУНМЦ МЗ РФ, 2002. – 80 с. Efremov AV. (2002).
Ефремов А.В. Геморрагические диатезы у де- тей. – М.: ГОУ ВУНМЦ МЗ РФ, 2002. – 80 с. Efremov AV. (2002).
4. Курдеко И.В., Назарова Р.В., Щербинина Л.Н. Варианты геморрагического синдрома у новорожденных // Омский научный вестник. – 2002. – Вып. 19 (Прил.). – С. 24–25.
5. Мазур Э.М. Тромбоцитопении // Патофизиоло- гия крови. – СПб., 2000. – С. 167–172.
6. Масчан А.А., Румянцев А.Г., Ковалева Л.Г. Ре- комендации Российского совета экспертов по диа- гностике и лечению больных первичной иммунной тромбоцитопенией // Онкогематология. – 2010. – № 3. – С. 36–45.
7. Шабалов Н.П., Иванов Д.О., Шабалова Н.Н. Гемостаз в динамике первой недели жизни, как отражение механизмов адаптации к внеутробной жизни новорожденного // Педиатрия. – 2000. – № 3. – С. 84–91.
– 2000. – № 3. – С. 84–91.
8. Beck N. (2009). Diagnostic hematology. London, 488 p.
9. Busset JB, Buchman GR, Nugen DJ. Gnarra DJ, Bomgaars LR, Blanchette VS, Wang YM, Nie K, Jun S. (2011). A randomized, double – blind study of romiplastin to determine its safety and efficacy i children with immune thrombocytopenia. Blood, 118 (1), 28-36. DOI: 10.1182/ blood-2010-10-313908
10. Chevuru SC, Sola MC, Theriaque DW, Hutson AD, Leung WC, Perez JA, Nelson RM, Kays DW, Christensen RD; Florida Collaborative Neonatology Research Group. (2002). Multicenter analysis of platelet transfusion usage among neonates on extracorporeal membrane oxygenation. Pediatrics, 109 (6), 89.
11. Handin RI, Loscalzo J. (1992). Hemostasis, thrombosis, fibrinolysis and cardiovascular disease. Heart Disease: A Textbook of Cardiovascular Medicine. Philadelphia, 767-1789.
(1992). Hemostasis, thrombosis, fibrinolysis and cardiovascular disease. Heart Disease: A Textbook of Cardiovascular Medicine. Philadelphia, 767-1789.
12. Portielje JE, Westendorp RG, Kluin-Nelemans HC, Brand A. (2001). Morbidity and mortality in adults with idiopathic thrombocytopenic purpura. Blood, 97 (9), 2549-2552.
Тромбоцитопеническая пурпура
Тромбоцитопеническая пурпура
Тромбоцитопеническая пурпура – это заболевание, которое характеризуется кровоизлияниями под кожу, повышенной кровоточивостью, возникающих в результате тромбоцитопении – снижения количества тромбоцитов в крови. Поскольку тромбоциты отвечают за свертываемость крови, снижение их количества в крови до 150×109/л приводит к ее низкой свертываемости, поэтому возникают обильные кровотечения. Само название болезни Purpura thrombocytopenica в переводе с латинского означает: purpura — пурпурный цвет, thrombocyte – тромбоциты, от греч. penia – бедность. Синоним: болезнь Верльгофа.
Само название болезни Purpura thrombocytopenica в переводе с латинского означает: purpura — пурпурный цвет, thrombocyte – тромбоциты, от греч. penia – бедность. Синоним: болезнь Верльгофа.
Тромбоцитопеническую пурпуру относят к заболеваниям группы геморрагических диатезов. Встречается эта болезнь с частотой 10-80 случаев на миллион жителей в год. Обнаруживается пурпура чаще всего в детском возрасте, обычно у детей 2-7 лет, но встречается даже у грудных детей. В возрасте до 10 лет мальчики и девочки болеют с одинаковой частотой, после 10 лет – девочки болеют в несколько раз чаще. Начинается пурпура, как правило, после вирусной или бактериальной инфекции.
Симптомы
- Кровоизлияния в кожу.
- Бледность кожи.
- Кровотечение из носа.
- Кровоточивость десен.
- Кишечные, желудочные кровотечения.
- У девочек – маточные кровотечения.
- Низкое давление.
- Повышение температуры до 38°С.

- Лимфаденопатия — увеличение лимфатических узлов.
- В 15-20% случаев – увеличение печени и селезенки.
Классификация
В зависимости от причин и механизма развития различают следующие виды заболевания:
- Идиопатическая тромбоцитопеническая пурпура (болезнь Верльгофа).
- Изоиммунная – из-за повторных переливаний крови или тромбоцитной массы, а также беременностей.
- Врожденная иммунная тромбоцитопеническая пурпура – из-за несовместимости крови матери и ребенка, обычно проходит к 4-5 месяцам жизни ребенка.
- Аутоиммунная тромбоцитопеническая пурпура – сочетается с анемией, системной красной волчанкой и др.
- Симптоматическая – наблюдается при дефиците витамина В12, лучевой болезни, некоторых инфекциях, приеме некоторых сильнодействующих лекарственных препаратов.
Сочетание пурпуры с эндокардитом, малярией, лейшманиозом может осложнить протекание этих инфекционных заболеваний.
Причины возникновения
Обычно причиной тромбоцитопенической пурпуры служит вирусная инфекция – в 80% случаев это грипп, ветрянка, корь, краснуха. Случается, что болезнь спровоцировала реакция на прививку при вакцинации. Врожденная форма болезни вызвана несовместимостью материнской крови и ребенка, наследственными заболеваниями крови или обмена веществ. Пурпура может возникнуть при лейкозе и других раковых заболеваниях крови.
Диагностика
Диагностика основана на фиксации характерных симптомов – носовых, желудочных, кишечных, маточных кровотечений, бледности кожи, высокой температуре. Проводятся эндотелиальные пробы – их положительный результат свидетельствует о пурпуре. Проведение лабораторных тестов (измерение времени кровотечения, определение степени ретракции сгустка крови и др.) – наиболее надежный способ диагностики тромбоцитопенической пурпуры.
Для дифференциальной диагностики тромбоцитопенической пурпуры от лейкоза, красной волчанки, тромбоцитопатии проводят иммунологические исследования, пункцию красного костного мозга, структурный анализ крови.
Лечение заболевания
Прежде всего, нужно обеспечить ребенку постельный режим. Обычно лечение тромбоцитопенической пурпуры проводят в больнице. При кровотечении десен и слизистой рта пища для ребенка должна быть охлажденной.
Для лечения назначаются глюкокортикоиды и иммунодепрессанты. Рассмотрим их применение поподробнее.
Преднизолон – применяется в течение 2-3 недель в дозировке 2 мг в сутки на каждый килограмм массы тела. Затем идет снижение дозы и отмена препарата. Иногда применяются короткие курсы по 7 дней с дозировкой 3 мг в сутки на каждый килограмм массы тела. Между такими курсами делают перерыв 5-7 дней. В большинстве случаев такая методика помогает, однако у некоторых пациентов после отмены преднизолона может возникнуть рецидив болезни.
Иммуноглобулины – применяются в сочетании с основными препаратами (обычно с глюкокортикоидами). Чаще всего назначается внутривенное введение Ig 0,4 мг/кг в сутки, курс – 5 дней. Если эти препараты не улучшают ситуацию, то применяют цитостатики.
При слабом эффекте глюкокортикоидов и иммуноглобулинов рассматривается целесообразность проведения спленэктомии – операции по удалению селезенки. Как правило, такую операцию проводят детям от 5 лет, помогает она в 70% случаев.
Смертность от тромбоцитопенической пурпуры составляет 1-2% случаев. Основная причина – кровоизлияние в головной мозг. За последние годы в связи с развитием медицины врачам удалось существенно сократить количество летальных исходов заболевания.
Профилактика
Никаких профилактических мер по предупреждению тромбоцитопенической пурпуры не разработано. Профилактика сводится к предотвращению возможных рецидивов. Среди возможных мер профилактики можно выделить особое внимание детям при вакцинации, индивидуальный подход к детям с повышенным риском заболевания. После полного выздоровления от пурпуры пациенты находятся на учете в течение 5 лет, регулярно сдают кровь для анализа количества тромбоцитов. При заболевании другой инфекционной болезнью необходимо проведение тщательного обследования.
Детская тромбоцитопения — Симптомы и причины
Обзор
Тромбоцитопения (throm-boe-sie-toe-PEE-nee-uh) — это состояние, при котором в крови недостаточно тромбоцитов. Тромбоциты (тромбоциты) — это бесцветные клетки крови, которые останавливают кровотечение за счет слипания и образования пробок при повреждениях кровеносных сосудов. В зависимости от причины низкий уровень тромбоцитов может привести или не привести к повышенному риску кровотечения.
Наиболее частой причиной тромбоцитопении у детей является иммунная тромбоцитопения (ИТП).Это происходит, когда иммунная система по ошибке атакует и уничтожает тромбоциты. Дети, у которых развивается ITP , часто имеют в анамнезе недавнюю вирусную инфекцию. Большинство детей выздоравливают после ITP без какого-либо лечения в течение шести месяцев. А пока им, возможно, придется избегать контактных видов спорта или других занятий, которые могут привести к травмам головы.
Менее распространенные причины тромбоцитопении у детей включают заболевания костного мозга, такие как лейкоз, или другие аутоиммунные состояния, такие как системная красная волчанка (СКВ) или наследственные заболевания костного мозга.
Симптомы
Некоторые дети с тромбоцитопенией никогда не испытывают симптомов кровотечения. Для тех, у кого есть симптомы, они могут включать:
- Легкие синяки
- Небольшие пурпурные пятна на коже (так называемые петехии или пурпура)
- Носовое кровотечение
- Кровотечение из десен
- Длительное кровотечение из мелких порезов
Дети с легкой формой тромбоцитопении могут вообще не иметь симптомов.
Причины
У детей может развиться тромбоцитопения, если костный мозг не производит достаточного количества тромбоцитов, организм разрушает слишком много тромбоцитов или селезенка удерживает слишком много тромбоцитов.
Эти проблемы могут возникнуть в результате:
- Заболевания, влияющие на иммунную систему
- Инфекции
- Наследственные болезни
- Воздействие определенных лекарств или токсинов
- Раки, такие как лейкемия или лимфома
Лечение детской тромбоцитопении в клинике Мэйо
2 июля 2020 г.
Показать ссылки- Тромбоцитопения.Национальный институт сердца, легких и крови. https://www.nhlbi.nih.gov/health-topics/thrombocytopenia. По состоянию на 27 апреля 2020 г.
- Kliegman RM, et al. Заболевания тромбоцитов и кровеносных сосудов. В: Учебник педиатрии Нельсона. 21-е изд. Эльзевир; 2020. https://www.clinicalkey.com. По состоянию на 27 апреля 2020 г.
- Despotovic JM. Подходить к ребенку с необъяснимой тромбоцитопенией. https://www.uptodate.
 com/contents/search. По состоянию на 27 апреля 2020 г.
com/contents/search. По состоянию на 27 апреля 2020 г. - Пруты РК (заключение эксперта).Клиника Майо. 3 июня 2020 г.
Детская тромбоцитопения
Иммунная тромбоцитопения у детей — что вам нужно знать
- Примечания по уходу
- Иммунная тромбоцитопения у детей
Этот материал нельзя использовать в коммерческих целях, в больницах или медицинских учреждениях. Несоблюдение может повлечь за собой судебный иск.
ЧТО НУЖНО ЗНАТЬ:
Что такое иммунная тромбоцитопения?
Иммунная тромбоцитопения — нарушение свертываемости крови. Иммунная тромбоцитопения может возникнуть, когда иммунная система вашего ребенка атакует и разрушает его тромбоциты. Это вызывает низкий уровень тромбоцитов. Тромбоциты — это клетки, которые способствуют свертыванию крови и останавливают кровотечение. Когда уровень тромбоцитов низкий, кровотечение может возникнуть в любом месте тела. Иммунная тромбоцитопения также может называться идиопатической тромбоцитопенией или ИТП. Большинство ИТП у детей выздоравливают через несколько недель или месяцев.Для лечения ИТП могут потребоваться лекарства, или может стать лучше. ИТП у детей может длиться от нескольких месяцев до лет и может перейти в хроническое состояние.
Когда уровень тромбоцитов низкий, кровотечение может возникнуть в любом месте тела. Иммунная тромбоцитопения также может называться идиопатической тромбоцитопенией или ИТП. Большинство ИТП у детей выздоравливают через несколько недель или месяцев.Для лечения ИТП могут потребоваться лекарства, или может стать лучше. ИТП у детей может длиться от нескольких месяцев до лет и может перейти в хроническое состояние.
Что увеличивает риск иммунной тромбоцитопении у моего ребенка?
- Недавняя вирусная инфекция или бактериальная инфекция, например корь или H. pylori
- Нарушение иммунной системы
- Лекарства, которые могут вызвать снижение уровня тромбоцитов, например антибиотики или лекарства от судорог
- Редко вакцины, например, от кори, паротита и краснухи
Каковы признаки и симптомы иммунной тромбоцитопении?
Признаки и симптомы вашего ребенка будут зависеть от количества его тромбоцитов.У него может не быть никаких симптомов, если уровень тромбоцитов в норме. У него может быть любое из следующего:
У него может быть любое из следующего:
- Синяки или красные или пурпурные пятна на коже или слизистых оболочках
- Кровотечение из десен или носа
- Кровь в моче или дефекации
- Обильное менструальное кровотечение у подростков
Как диагностируется иммунная тромбоцитопения?
Лечащий врач вашего ребенка осмотрит его и спросит о его симптомах. Расскажите ему о любых лекарствах или добавках, которые принимает ваш ребенок.Будут сделаны анализы крови, чтобы проверить уровень тромбоцитов у вашего ребенка и скорость его свертывания.
Как лечится иммунная тромбоцитопения?
Лечащий врач вашего ребенка решит, нужно ли ему лечение. Лечение будет зависеть от уровня тромбоцитов и симптомов у вашего ребенка. Ему потребуется тщательный мониторинг уровня тромбоцитов, независимо от лечения. Ему мне понадобится любое из следующего:
- Лекарства могут быть назначены для предотвращения разрушения тромбоцитов иммунной системой вашего ребенка.
 Также могут быть назначены лекарства для повышения уровня тромбоцитов и предотвращения кровотечений. Лекарства можно вводить в виде таблеток или внутривенно.
Также могут быть назначены лекарства для повышения уровня тромбоцитов и предотвращения кровотечений. Лекарства можно вводить в виде таблеток или внутривенно. - Переливание тромбоцитов может быть назначено, если уровень тромбоцитов у вашего ребенка низкий. Переливание тромбоцитов также может помочь остановить сильное кровотечение. Вашему ребенку может потребоваться переливание тромбоцитов перед операцией или процедурами, чтобы помочь его свертыванию крови.
- Операция по удалению селезенки вашего ребенка требуется редко, но может быть сделана, чтобы предотвратить разрушение тромбоцитов в его организме.
Что я могу сделать, чтобы ухаживать за своим ребенком?
- Уход за кожей ребенка. Используйте мягкую зубную щетку, чтобы предотвратить кровоточивость десен вашего ребенка. Попросите ребенка использовать бальзам для губ, чтобы губы не растрескались. Используйте мягкую мочалку во время принятия ванны или душа. Нанесите лосьон на его сухую кожу.
 Не стригите его ногти слишком коротко. Пусть ваш ребенок будет носить тапочки или обувь, чтобы защитить его ноги.
Не стригите его ногти слишком коротко. Пусть ваш ребенок будет носить тапочки или обувь, чтобы защитить его ноги. - Не позволяйте ребенку заниматься деятельностью, которая может привести к травме. Спросите у лечащего врача вашего ребенка, какие занятия безопасны для него.Ваш ребенок может не иметь возможности заниматься контактными видами спорта, такими как хоккей, футбол или бокс.
- Не давайте ребенку аспирин или НПВП. Эти лекарства могут препятствовать нормальной работе тромбоцитов. Это может вызвать у него кровотечение и синяки.
- Уход за порезами, царапинами или носовым кровотечением у вашего ребенка. Сильно и равномерно надавливайте на порезы или царапины. Используйте марлю или чистое полотенце. Если возможно, поднимите часть тела выше уровня сердца. Если у вашего ребенка кровотечение из носа, ущипните его нос и ноздри.Делайте это, пока кровотечение не остановится.
- Попросите ребенка иметь при себе удостоверение здоровья.
 Пусть он носит украшения или носит карточку, на которой написано, что у него иммунная тромбоцитопения. Спросите у лечащего врача, где взять эти предметы.
Пусть он носит украшения или носит карточку, на которой написано, что у него иммунная тромбоцитопения. Спросите у лечащего врача, где взять эти предметы.
Позвоните 911 по любому из следующих номеров:
- Ваш ребенок упал и ударился головой.
- У вашего ребенка припадок.
- Ваш ребенок не может быть разбужен.
- У вашего ребенка проблемы с дыханием.
Когда мне следует немедленно обратиться за помощью?
- У вашего ребенка внезапная сильная головная боль.
- Ваш ребенок сбит с толку или у него проблемы со зрением, разговором или слухом.
- Ваш ребенок неоднократно рвет.
- У вашего ребенка на голове выпуклое мягкое пятно (родничок).
- У вашего ребенка внезапная слабость, онемение или проблемы с равновесием и движением.
- Кровотечение у вашего ребенка не прекращается или усиливается.
- Рука или нога вашего ребенка выглядит больше, ему тепло и больно.

Когда мне следует связаться с лечащим врачом моего ребенка?
- У вашего ребенка высокая температура.
- У вашего ребенка кровотечение из десен, рта или носа.
- У вашего ребенка боли в животе.
- У вашего ребенка кровь в моче или дефекации.
- Вы видите новые синяки или маленькие красные или пурпурные пятна на коже вашего ребенка.
- У вас есть вопросы или опасения по поводу состояния вашего ребенка или ухода за ним.
Соглашение об уходе
Вы имеете право помогать планировать уход за своим ребенком. Узнайте о состоянии здоровья вашего ребенка и о том, как его можно лечить.Обсудите варианты лечения с поставщиками медицинских услуг вашего ребенка, чтобы решить, какое лечение вы хотите для своего ребенка. Вышеуказанная информация носит исключительно учебный характер. Он не предназначен для использования в качестве медицинского совета по поводу индивидуальных состояний или лечения. Поговорите со своим врачом, медсестрой или фармацевтом перед тем, как следовать любому лечебному режиму, чтобы узнать, безопасно ли оно для вас и эффективно.
© Copyright IBM Corporation 2020 Информация предназначена только для использования конечным пользователем и не может быть продана, распространена или иным образом использована в коммерческих целях.Все иллюстрации и изображения, включенные в CareNotes®, являются собственностью A.D.A.M., Inc. или IBM Watson Health
, защищенной авторским правом. Дополнительная информация
Всегда консультируйтесь со своим поставщиком медицинских услуг, чтобы убедиться, что информация, отображаемая на этой странице, применима к вашим личным обстоятельствам.
Заявление об отказе от ответственности за медицинское обслуживание
Узнайте больше об иммунной тромбоцитопении у детей
Сопутствующие препараты
IBM Watson Micromedex
Лимфома Действие | Тромбоцитопения (низкий уровень тромбоцитов)
,00Что такое тромбоцитопения?
Тромбоцитопения — это нехватка тромбоцитов (также называемых «тромбоцитами») в крови.
Тромбоциты — это тип клеток крови, участвующих в свертывании крови. Когда вы порезаетесь или повреждаете кровеносный сосуд, тромбоциты заполняют отверстие, образуя тромбоцитарную пробку. Факторы свертывания крови (белки в крови) затем связывают все вместе, пока область заживает.
Рисунок: Тромбоциты
Тромбоциты вырабатываются в костном мозге (губчатом центре некоторых костей). Обычно они остаются в кровотоке около 10 дней, прежде чем удаляются селезенкой.Костный мозг все время работает, чтобы производить новые тромбоциты. Это работает тяжелее, если тромбоциты необходимы для остановки кровотечения где-то в вашем теле.
Если у вас низкое количество тромбоцитов, вам сложнее сформировать сгусток крови. Это означает, что вы можете истечь кровью дольше, чем обычно, если порежетесь. Вы также можете получить синяк быстрее, чем обычно.
Если у вас низкое количество тромбоцитов, у вас «тромбоцитопения».
К началу
Сколько тромбоцитов мне нужно?
Количество тромбоцитов в крови измеряется с помощью теста, называемого полным анализом крови (FBC). 9 / л. Это немного сложно, поэтому врачи и медсестры обычно просто ссылаются на число (например, количество тромбоцитов 150).
9 / л. Это немного сложно, поэтому врачи и медсестры обычно просто ссылаются на число (например, количество тромбоцитов 150).
К началу
Тромбоцитопения может возникнуть, если костный мозг не производит достаточного количества тромбоцитов или если тромбоциты используются или разрушаются быстрее, чем костный мозг может их заменить.
У людей с лимфомой тромбоцитопения может возникнуть из-за:
Лимфома в костном мозге
Если клетки лимфомы находятся в костном мозге, они занимают место, которое обычно используется для производства здоровых клеток крови.Это может снизить количество тромбоцитов, вырабатываемых костным мозгом, и у вас разовьется тромбоцитопения.
Тромбоцитопения, вызванная лимфомой в костном мозге, часто начинает улучшаться, когда лечение лимфомы начинает работать и количество лимфомных клеток уменьшается.
Лечение лимфомы
Хотя цель химиотерапии — убить клетки лимфомы, поражаются и некоторые здоровые клетки. Это могут быть клетки костного мозга, которые производят новые тромбоциты.Если эти клетки не производят достаточно тромбоцитов, чтобы заменить те, которые отмирают естественным путем, количество тромбоцитов падает.
Это могут быть клетки костного мозга, которые производят новые тромбоциты.Если эти клетки не производят достаточно тромбоцитов, чтобы заменить те, которые отмирают естественным путем, количество тромбоцитов падает.
Количество тромбоцитов в крови обычно начинает падать через 7-10 дней после химиотерапии и достигает минимального значения примерно через 2 недели после лечения. Уровень тромбоцитов постепенно возвращается к норме через 4-5 недель.
Не все схемы химиотерапии (комбинации препаратов) вызывают тромбоцитопению.
Лучевая терапия может вызвать тромбоцитопению, если она используется для лечения большой площади или если она проводится в сочетании с химиотерапией.
Некоторые виды терапии антителами и таргетные препараты также могут вызывать тромбоцитопению.
Спленомегалия
Некоторые тромбоциты не только циркулируют в крови, но и хранятся в селезенке. Поскольку этих тромбоцитов нет в вашем кровотоке, они не способствуют свертыванию и не учитываются при подсчете тромбоцитов. Если ваша селезенка больше обычного (спленомегалия), там собирается больше тромбоцитов. В результате в кровотоке остается меньше тромбоцитов, чем обычно.
Если ваша селезенка больше обычного (спленомегалия), там собирается больше тромбоцитов. В результате в кровотоке остается меньше тромбоцитов, чем обычно.
Иммунная тромбоцитопения
Иногда лимфома может заставить вашу иммунную систему вырабатывать антитела против ваших собственных клеток.Эти антитела известны как «аутоантитела».
Если аутоантитела прилипают к тромбоцитам, тромбоциты разрушаются при прохождении через селезенку. Если ваш костный мозг не может производить новые тромбоциты достаточно быстро, чтобы заменить разрушенные, количество тромбоцитов падает и развивается тромбоцитопения. Этот тип тромбоцитопении известен как «иммунная тромбоцитопения». Это необычно для людей с лимфомой Ходжкина и большинства типов неходжкинской лимфомы, но может поражать до 1 из 10 человек с хроническим лимфолейкозом (ХЛЛ).
К началу
У большинства людей с низким уровнем тромбоцитов нет никаких симптомов. Это потому, что ваше тело имеет встроенный резерв с гораздо большим количеством тромбоцитов, чем вам нужно в повседневной жизни.
Если количество тромбоцитов упадет до очень низкого уровня, вы можете заметить некоторые симптомы и признаки. Общее руководство по тому, что вы можете испытывать при разном количестве тромбоцитов:
- слегка пониженное количество тромбоцитов (более 50): у вас, вероятно, не будет никаких симптомов
- Низкое количество тромбоцитов (от 30 до 50): синяки могут появиться быстрее и кровоточить дольше, если порезаться.
- очень низкое количество тромбоцитов (от 10 до 30): у вас может начаться кровотечение после очень незначительных травм, которые обычно не кровоточат, кровоточат дольше, чем обычно, и более легко образуются синяки
- чрезвычайно низкое количество тромбоцитов (ниже 10): у вас есть риск кровотечения даже без очевидной причины.
Если у вас низкое количество тромбоцитов, вызывающее кровотечение, у вас также может развиться анемия.
Обратитесь к своей медицинской бригаде, если у вас появятся какие-либо из следующих симптомов:
- Носовое кровотечение
- кровоточат десна после чистки зубов
- обильные месячные у женщин
- кровотечение дольше обычного после пореза или царапины
- кровоподтеки легче, чем обычно
- маленькие красные или фиолетовые пятна, называемые «пурпура» или «петехии» на коже (часто на ногах), губах или во рту
- кровь в рвоте
- кровь в моче
- Кровь в ваших фекалиях (это может быть очевидно, ярко-красная кровь или может сделать ваши фекалии черными и липкими)
- постоянная головная боль, помутнение зрения или изменение уровня сознания.

Если у вас началось кровотечение, немедленно обратитесь в больницу.
Рисунок: Пурпура (маленькие красные или фиолетовые пятна) на ногах
Рисунок: Петехии (крошечные красные или пурпурные пятна) на внутренней стороне рта
К началу
Тромбоцитопения часто бывает недолгой, и многие люди с низким количеством тромбоцитов вообще не нуждаются в лечении. Однако, если у вас очень низкий уровень тромбоцитов или вы подвержены особому риску кровотечения, вам может потребоваться лечение.Это может включать:
Лечение иммунной тромбоцитопении отличается, поскольку оно плохо реагирует на переливание тромбоцитов.
Изменения в ваших лекарствах
Некоторые лекарства, в том числе разжижающие кровь, некоторые антибиотики и некоторые лекарства, которые можно купить без рецепта (например, аспирин), могут вызывать тромбоцитопению или повышать риск кровотечения после развития тромбоцитопении. Ваша медицинская бригада проверит, какие лекарства вы принимаете, и остановит или скорректирует дозу тех, которые могут повлиять на количество тромбоцитов.
Ваша медицинская бригада проверит, какие лекарства вы принимаете, и остановит или скорректирует дозу тех, которые могут повлиять на количество тромбоцитов.
Если вы проходите химиотерапию и у вас очень низкое количество тромбоцитов, доза химиотерапии может быть уменьшена или у вас может быть более длительный перерыв между курсами лечения. Иногда ваш режим химиотерапии может быть изменен.
Переливание тромбоцитов
Переливания тромбоцитов аналогичны переливаниям крови при анемии. Вам может потребоваться переливание тромбоцитов, если:
- у вас очень низкое количество тромбоцитов (менее 10)
- у вас очень низкое количество тромбоцитов (менее 20) и жар
- у вас низкое или очень низкое количество тромбоцитов (от 30 до 50) и у вас кровотечение
- у вас низкое количество тромбоцитов (обычно менее 50), и вам необходимо сделать операцию или другую медицинскую процедуру, которая подвергает вас риску кровотечения.
Переливания тромбоцитов нацелены на увеличение количества тромбоцитов, достаточное для остановки кровотечения или снижения риска кровотечения. Поскольку тромбоциты израсходуются, эффект длится всего несколько дней.
Поскольку тромбоциты израсходуются, эффект длится всего несколько дней.
Другие виды лечения
Иногда лекарство, называемое «транексамовая кислота», может использоваться вместе с переливанием тромбоцитов или вместо него. Он предотвращает или уменьшает кровотечение, не давая сгусткам крови разрушаться.
Иногда вам могут потребоваться другие методы лечения, чтобы помочь свертыванию крови, например инъекция витамина К или вливание свежезамороженной плазмы (аналогично переливанию крови).
Лечение иммунной тромбоцитопении
Если ваша тромбоцитопения вызвана аутоантителами, разрушающими ваши тромбоциты, переливание тромбоцитов обычно не работает. Вместо этого вас, вероятно, будут лечить стероидами, такими как преднизолон. Доза стероида для начала высока, что может вызвать раздражение желудка. Вам могут дать другое лекарство для защиты желудка. Как только ваш уровень тромбоцитов находится под контролем, доза стероидов снижается.
Стероиды эффективны для большинства людей с аутоиммунной тромбоцитопенией. Если стероиды неэффективны, другие возможные методы лечения включают заместительную иммуноглобулиновую терапию, лечение антителами с помощью ритуксимаба или спленэктомию (удаление селезенки). Некоторым людям необходимо лечение препаратами, которые подавляют (ослабляют) вашу иммунную систему (иммунодепрессанты).
Если стероиды неэффективны, другие возможные методы лечения включают заместительную иммуноглобулиновую терапию, лечение антителами с помощью ритуксимаба или спленэктомию (удаление селезенки). Некоторым людям необходимо лечение препаратами, которые подавляют (ослабляют) вашу иммунную систему (иммунодепрессанты).
Если ваш уровень тромбоцитов по-прежнему не улучшается, вам может потребоваться лечение препаратом, называемым «агонистом рецепторов тромбопоэтина». Тромбопоэтин — это гормон (химический посредник), который сообщает костному мозгу, что нужно производить больше тромбоцитов.Агонисты рецепторов тромбопоэтина — это лекарства, имитирующие эффекты тромбопоэтина. Они могут вас лечить, если:
- Иммунная тромбоцитопения
- Количество тромбоцитов не поддается лечению другими препаратами
- Вы очень больны
- у вас высокий риск кровотечения и
- Вам необходимы частые курсы лечения тромбоцитопении.
Наверх
Снижение риска кровотечения
Если у вас низкий уровень тромбоцитов, вы можете предпринять несколько простых мер предосторожности, чтобы снизить риск кровотечения.
Продукты питания, напитки и лекарства
- Старайтесь избегать еды, которая может вызвать кровотечение изо рта (например, чипсов).
- Ограничьте количество употребляемого алкоголя (это может усилить кровотечение).
- Не принимайте аспирин или другие разжижающие кровь лекарства, если только ваш врач не сказал вам об этом.
- Не используйте клизмы или суппозитории.
Деятельность
- Будьте особенно осторожны, чтобы не порезаться ножами или ножницами.
- Избегайте спорта с высокой ударной нагрузкой (например, бег на длинные дистанции) и контактных видов спорта (например, регби).
- Надевайте перчатки, длинные рукава и длинные брюки, чтобы защитить себя от царапин и порезов при работе в саду или при выполнении домашних работ.
- Будьте осторожны, чтобы не обжечься при глажении и приготовлении пищи.
- Носите обувь на улице.
Гигиена
- Используйте бальзам для губ и увлажняющий крем, чтобы предотвратить пересыхание губ и кожи.

- Осторожно чистите зубы мягкой зубной щеткой и избегайте использования зубной нити, чтобы предотвратить кровоточивость десен.
- По возможности не выполняйте никаких стоматологических операций.
- Не сморкайтесь слишком сильно или слишком часто.
- Используйте электрическую бритву вместо влажного бритья.
- Используйте гигиенические прокладки вместо тампонов.
- Постарайтесь не напрягаться при пользовании туалетом.
- Используйте смазку на водной основе во время секса. (Вам могут посоветовать полностью отказаться от секса, если количество тромбоцитов ниже 50.)
Что делать при кровотечении
- Сохраняйте спокойствие.
- Сядьте или лягте.
- Если можете, надавите на травму.
- Используйте пакет со льдом, чтобы замедлить кровотечение.
- Если возможно, приподнимите травму выше уровня сердца.
- Обратитесь в свою больницу.
Наверх
Иммунная тромбоцитопения (ИТП)
Заявление об ограничении ответственности Это руководство было разработано для принятия клинических решений медицинским, медсестринским и смежным медицинским персоналом детской больницы Перта. R Ознакомьтесь с полным отказом от ответственности отделения неотложной помощи PCH. |
Цель
Для руководства медицинским персоналом PCH в оценке и лечении иммунной тромбоцитопении (ИТП).
Определение 1-3
ИТП — необычное заболевание, которым страдает 1–3 из 10 000 детей. Количество тромбоцитов составляет 9 / л, а может достигать 9 / л.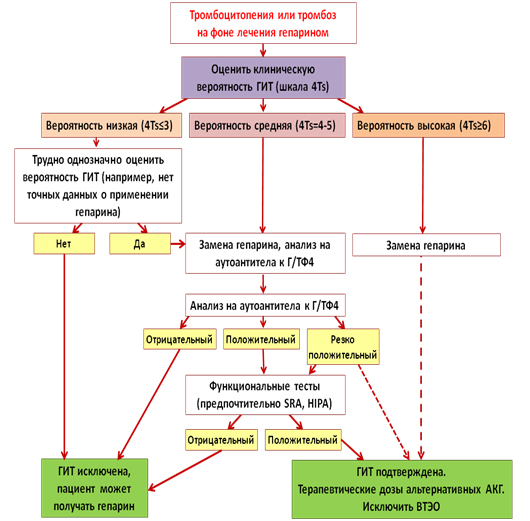 У детей наблюдаются петехии, пурпура (синяки) и иногда кровотечение из слизистой оболочки. Редко может возникнуть ректальное кровотечение или гематурия.Риск внутричерепного кровотечения (ICH) составляет
У детей наблюдаются петехии, пурпура (синяки) и иногда кровотечение из слизистой оболочки. Редко может возникнуть ректальное кровотечение или гематурия.Риск внутричерепного кровотечения (ICH) составляетФон 1-5
- ИТП — наиболее частая причина тромбоцитопении в детском возрасте.
- Это результат иммуноопосредованного разрушения тромбоцитов, часто вызванного вирусными инфекциями, и других проблем коагуляции нет.
- Дети находятся в возрасте от 2 до 10 лет, с пиком заболеваемости в дошкольном возрасте.
- ИТП можно разделить на два клинических синдрома:
- Острый ИТП — 90% детей.У этих пациентов остро появляются спонтанные синяки, и ИТП проходит в течение нескольких недель или месяцев после постановки диагноза.
- Хроническая ИТП — 10% детей. Это длится более 6 месяцев, а часто и более 12 месяцев. Изложение может быть более коварным.
Оценка
- Здоровые дети с петехиями и пурпурой; кровотечение слизистой оболочки — нечасто.

- Клиническая оценка направлена на за исключением других причин петехий / пурпуры и тромбоцитопении e.г. злокачественные новообразования.
- Тяжесть заболевания определяется клинической картиной, не количеством тромбоцитов, которое может быть <20 x 10 9 / л
- Внутримозговое кровоизлияние редко, но его следует рассматривать у любого пациента с ИТП с неврологическими симптомами или признаками.
Учитывать повышенные факторы риска внутричерепного кровотечения (ICH)
|
История
- Петехии и пурпура — вид, степень тяжести, продолжительность.
- Кровотечение слизистой оболочки — носовое кровотечение, гематурия, ректальное кровотечение, тяжесть и продолжительность.
- Предыдущие проблемы с гемостазом после процедур.
- Системные симптомы — особенно любые недавние вирусные инфекции за последние 6 недель.
- ICH следует рассматривать, если есть симптомы или признаки со стороны ЦНС, такие как летаргия, головная боль, рвота, снижение уровня сознания.
- Возможная системная красная волчанка ( SLE ) — светочувствительная сыпь, артрит, миалгия, язвы во рту, выпадение волос, сухость в глазах или во рту, усталость, потеря веса, лихорадка. Учтите, что у детей старшего возраста этническое происхождение высокого риска (например, аборигены, азиаты, африканцы, маори).
- Возможное злокачественное новообразование : хроническая боль, лихорадка, потеря веса, бледность.

- Рецидивирующие инфекции: наводят на мысль об иммунодефиците.
- Недавняя вакцинация живым вирусом (e.г. MMR).
- Лекарства: хинин, пенициллин, дигоксин, противоэпилептические средства, салицилаты, гепарин, варфарин.
- Семейный анамнез: СКВ, тромбоцитопения или другие гематологические или иммунологические нарушения.
- Коморбидные состояния, которые могут увеличить риск кровотечения.
- Факторы образа жизни, которые могут представлять риск травм и кровотечений.
Экзамен
- Обычно красивый ребенок с нормальным наблюдением
- Признаки кровотечения: документально подтвердить расположение и размер пурпуры, области петехий.Поищите кровотечение из слизистой оболочки, проверьте кровоизлияние в сетчатку.
- Не должно быть бледности, лимфаденопатии или гепатоспленомегалии. Эти результаты НЕ согласуются с ITP .
- Нет признаков инфекции
- Полное документированное обследование ЦНС
- Дисморфические признаки: наводящие на мысль о врожденном синдроме, например Синдром Фанкони, синдром тромбоцитопенического отсутствия лучевой кости (TAR).

Расследования
- Общий анализ мочи на гематурию при каждом обращении:
- Транексамовая кислота противопоказана при гематурии
- Гематурия связана с повышенным риском ICH.
- Изображение полной крови (FBP): показывает тромбоцитопению (может быть <20 x 10 9 / л), нормальный гемоглобин, нормальное количество лейкоцитов
- Мазок крови должен быть просмотрен лабораторным гематологом, чтобы подтвердить, что характеристики пленки соответствуют клиническому диагнозу ITP .
- У пациентов с симптомами и признаками ЦНС следует рассмотреть возможность проведения срочной визуализации головного мозга
- МНО, АЧТВ или тесты на свертываемость не требуются, если не подозревается значительное кровотечение или неслучайное повреждение (NAI)
- Аспират костного мозга требуется редко и рассматривается только в том случае, если диагноз не определен и необходимо исключить гематологическое злокачественное новообразование.

Дифференциальные диагнозы
Следует рассмотреть широкий дифференциальный диагноз, особенно для детей старшего возраста.
- Системная красная волчанка (например, СКВ).
- Гематологические злокачественные новообразования (например, лейкемия).
- Апластическая анемия.
- Инфекции — вирусы, менингококковая инфекция.
- Тромбоцитопения, вызванная лекарственными средствами.
- Гемолитико-уремический синдром.
- Другие нарушения свертывания крови e.г. диссеминированное внутрисосудистое свертывание (ДВС).
Менеджмент
- ИТП у большинства педиатрических пациентов спонтанно исчезнет без какого-либо лечения в течение 6 месяцев.
- Решения о лечении должны основываться на кровотечении, а не на количестве тромбоцитов.
- Приведенная ниже таблица использовалась в исследованиях педиатрических пациентов с ИТП для принятия решений о терапии.

Таблица 1: Оценка тяжести кровотечения у пациентов с ИПТ 4,5
| 0 | Нет | Нет новых кровотечений | Обычно лечение не требуется |
| 1 | Незначительный | Небольшое количество петехий (всего ≤ 100) и / или ≤5 небольших синяков (≤3 см в диаметре), кровотечения через слизистую оболочку отсутствуют | Обычно лечение не требуется |
| 2 | мягкий | Многие петехии (всего> 100) и / или большие синяки (> 3 см в диаметре) | Обычно лечение не требуется |
| 3A | Низкий риск умеренный | Кровяные корки в ноздрях, безболезненная оральная пурпура, оральные / небные петехии, буккальная пурпура только вдоль моляров, легкое носовое кровотечение ≤5 мин | Обычно лечение не требуется |
| 3B | Высокий риск умеренный | Носовое кровотечение> 5 мин, гематурия, гематохезия, болезненная пурпура полости рта, значительная меноррагия | Обычно показано лечение |
| 4 | Тяжелая | Кровотечение слизистой оболочки или подозрение на внутреннее кровотечение (мозг, легкие, мышцы, суставы и т. Д.)), который требует немедленной медицинской помощи или вмешательства Д.)), который требует немедленной медицинской помощи или вмешательства | Обычно показано лечение |
| 5 | Опасность для жизни / со смертельным исходом | Документированное внутричерепное кровотечение или опасное для жизни или смертельное кровотечение в любом месте | Обычно показано лечение |
Ведение пациентов с риском тяжелого кровотечения от нулевого до низкого / умеренного (степень от 0 до 3A)
Эти пациенты:- Имеются кожные проявления ИТП или кровотечение слизистой оболочки в анамнезе, которое остановилось на момент клинической оценки и не было продолжительным (см. Таблицу 1).
- Обычно можно лечить консервативно без лечения, с последующим амбулаторным наблюдением.
- Может рассматриваться для лечения в исключительных обстоятельствах, таких как неизбежная поездка за границу, подросток с проблемами самооценки или высокий риск травмы.

Ведение пациентов с особыми соображениями / социальными проблемами
- Эти пациенты:
- Меноррагия, неизбежное заграничное путешествие, проблемы с самооценкой, высокий риск травмы, социальные проблемы
- Может потребоваться лечение стероидами и / или госпитализация в рамках общей педиатрии.
Ведение пациентов с повышенным риском ICH
Пациентов с:
- Гематурия, длительное / эпизодическое кровотечение слизистой оболочки и / или кровотечение из нескольких участков в анамнезе должны рассматриваться и контролироваться в соответствии с уровнем риска 3B высокий-средний
- травма головы, НПВП в предыдущие 5 дней, возможно, потребуется лечение стероидами и / или госпитализация в рамках общей педиатрии.
Ведение пациентов с высоким-умеренным риском (степень 3B)
Эти пациенты:- носовое кровотечение> 5 минут, гематурия, ректальное кровотечение, болезненная пурпура в полости рта или значительная меноррагия
- обычно требуют лечения
- Следует принять в бригаду гематологов / онкологов.

Сообщите педиатру общего профиля, если пациент ему известен.
Лечение высокого-среднего риска
- Не влияет на естественное течение ИТП, но может резко повысить количество тромбоцитов
- Следует обсудить с гематологом / онкологом Дежурный консультант
Таблица 2
| 1. Общая продолжительность носового кровотечения> 5 и <20 минут | Допускается к наблюдению
|
| 2.Общая продолжительность носового кровотечения> 20 минут <60 минут |
|
| 3. Общая продолжительность> 60 минут |
|
4. Носовые кровотечения любой продолжительности с множественными кровотечениями на слизистой оболочке Носовые кровотечения любой продолжительности с множественными кровотечениями на слизистой оболочке |
|
Таблица 3
| 1.Преднизолон | 4 мг / кг / день перорально (максимум 200 мг) в 2-4 приема в течение 4 дней 4,7 |
|
| 2. IVIg | См. Дозы ниже. |
|
| 3. Транексамовая кислота | 25 мг / кг перорально (максимум до 1,5 г) три раза в день в течение 3-5 дней с осмотром врача на 5 день. 4,6 | Считается дополнительным средством к стероидам и внутривенным иммуноглобулинам ( c при гематурии ):
|

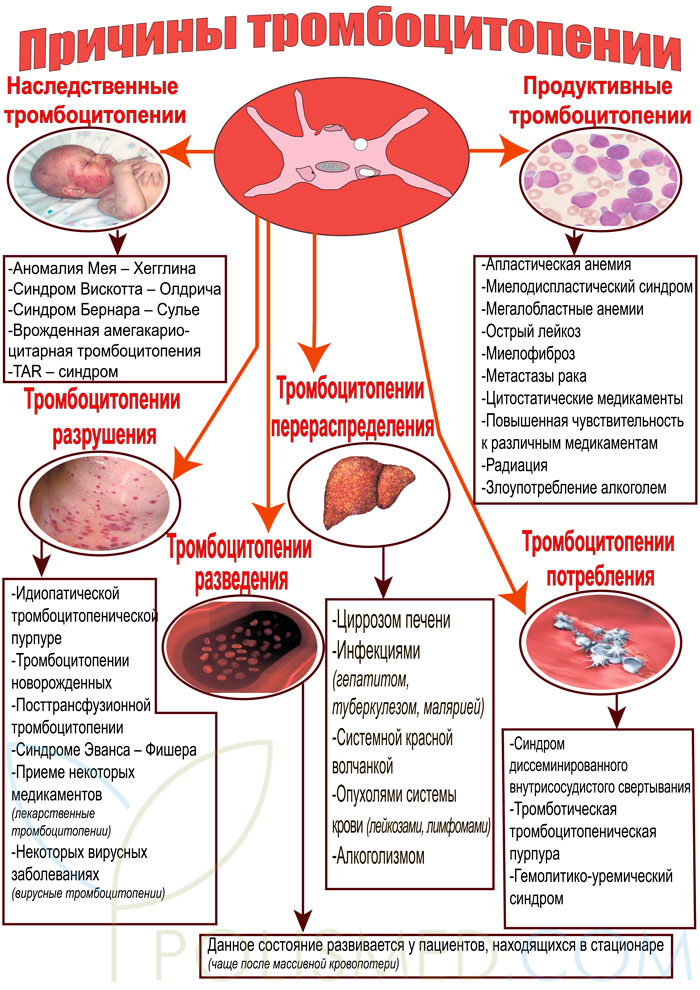


 com/contents/search. По состоянию на 27 апреля 2020 г.
com/contents/search. По состоянию на 27 апреля 2020 г. Также могут быть назначены лекарства для повышения уровня тромбоцитов и предотвращения кровотечений. Лекарства можно вводить в виде таблеток или внутривенно.
Также могут быть назначены лекарства для повышения уровня тромбоцитов и предотвращения кровотечений. Лекарства можно вводить в виде таблеток или внутривенно. Не стригите его ногти слишком коротко. Пусть ваш ребенок будет носить тапочки или обувь, чтобы защитить его ноги.
Не стригите его ногти слишком коротко. Пусть ваш ребенок будет носить тапочки или обувь, чтобы защитить его ноги. Пусть он носит украшения или носит карточку, на которой написано, что у него иммунная тромбоцитопения. Спросите у лечащего врача, где взять эти предметы.
Пусть он носит украшения или носит карточку, на которой написано, что у него иммунная тромбоцитопения. Спросите у лечащего врача, где взять эти предметы.


 Это не строгие протоколы, и они не заменяют заключение старшего врача . Всегда следует руководствоваться здравым смыслом. Никогда не следует полагаться на эти клинические рекомендации как на замену надлежащей оценки конкретных обстоятельств каждого случая и потребностей каждого пациента. Перед тем, как следовать каким-либо рекомендациям, клиницисты должны также учитывать имеющийся у них уровень квалификации и местную политику.
Это не строгие протоколы, и они не заменяют заключение старшего врача . Всегда следует руководствоваться здравым смыслом. Никогда не следует полагаться на эти клинические рекомендации как на замену надлежащей оценки конкретных обстоятельств каждого случая и потребностей каждого пациента. Перед тем, как следовать каким-либо рекомендациям, клиницисты должны также учитывать имеющийся у них уровень квалификации и местную политику.








